Bức tranh kháng thuốc do Plasmodium spp ngày càng nghiêm trọng
Hơn một thập niên qua, thế giới đã có nhiều tiến bộ quan trọng chống lại căn bệnh sốt rét – và đối mặt với tình hình sốt rét kháng thuốc - vốn dĩ từ lâu được xem là “vua của các bệnh” bởi sự tổng hòa các triệu chứng và biến chứng của nhiều bệnh nội khoa và truyền nhiễm khác nhau trên cùng một cơ thể bệnh nhân, nhất là khi bệnh nhân sốt rét ác tính (SRAT). Kể từ năm 2000, tử vong do sốt rét đã giảm hơn 25%. Với 104 quốc gia có sốt rét lưu hành, 50 trong số 99 quốc gia đang có lan truyền sốt rét đang tiếp cận dần đến mục tiêu của Hội đồng Y tế thế giới 2015 về giảm tỷ lệ mắc mới hơn 75%.
Dù đã có sự can thiệp tích cực của biện pháp phòng chống vector, song hành cùng tiếp cận các phương pháp và kỹ thuật chẩn đoán hiện đại chính xác và điều trị thuốc hiệu quả nhưng sốt rét vẫn cướp đi sinh mạng hàng trăm người trên toàn thế giới mỗi năm, chủ yếu là trẻ em nhỏ và phụ nữ mang thai ở vùng cận sa mạc Sahara, châu Phi và Đông Nam Á. Mỗi năm có hơn 200 triệu ca mắc mới xảy ra. Đồng thời, các dẫn liệu gần đây cho thấy nhiều thách thức và có nguy cơ đe dọa các thành quả do tình trạng côn trùng kháng hóa chất và ký sinh trùng sốt rét kháng thuốc có hiệu lực cao. !important; |
Thành quả các chiến lược phòng chống sốt rét (PCSR) đạt được không thể không kể đến tác dụng của thuốc sốt rét (SR), nên công tác giám sát thường quy tình hình nhạy kháng thuốc là một trong những điểm hoạt động then chốt làm giảm tỷ lệ mắc bệnh và tử vong. Tình trạng Plasmodium falciparum (P. falciparum) đa kháng thuốc lan rộng nghiêm trọng trên thế giới và khu vực Tây Thái Bình Dương là một trở ngại kỹ thuật cho việc lựa chọn thuốc. Hiện tượng KSTSR kháng artemisinins và artesunate hoặc dẫn chất khác tại khu vực biên giới Thái Lan – Campuchia, và gần đây đã lan rộng ra 4 quốc gia Campuchia, Thái Lan, Việt Nam và Myanmar trong 5 năm qua như thể cảnh báo sớm chúng ta đang mất dần vũ khí tối ưu nhất chống lại ký sinh trùng. Việt Nam chia sẻ một dải biên giới với Lào, Trung Quốc, đặc biệt với quốc gia Campuchia (được xem là núi lửa ẩn chứa KSTSR kháng thuốc), P. falciparum đã kháng cao với chloroquine, fansidar, quinine, mefloquine và giảm đáp ứng với nhiều loại thuốc hiện dùng, kể cả nhóm thuốc phối hợp ACTs.
Nghiên cứu và cho ra đời một thuốc ACTs thế hệ mới ARCO (Artemisinin-Naphthoquine)
Liên quan dược lý học đến thuốc ACTs mới (Biệt dược ARCO)
Một số nét sơ lược về thuốc đi cùng pyronaridine
Pyronaridine là một thuốc tổng hợp vào năm 1970s tại Viện Nghiên cứu bệnh ký sinh trùng Trung Quốc (Institute of Chinese Parasitic Disease) và đã đưa vào sử dụng tại Trung Quốc hơn 30 năm qua để điều trị SR. Pyronaridine có hiệu lực cao chống lại P. falciparum, kể cả chủng đã kháng với thuốc chloroquine. Các nghiên cứu trên các mô hình động vật khác nhau chỉ ra rằng pyronaridine có hiệu quả chống lại các chủng đã kháng với các thuốc SR khác trước đó, kể cả chloroquine. Kháng với thuốc pyronaridine đơn thuần dường như đã xuất hiện chậm và càng chậm hơn nữa khi pyronaridine được sử dụng phối hợp với các thuốc chống SR khác, đặc biệt artesunate. Độc tính của pyronaridine nhìn chung ít hơn so với chloroquine, mặc dù bằng chứng cho thấy có gây độc cho phôi trên các gặm nhấm, nên đã đưa ra cảnh báo dùng thuốc khi phụ nữ có mang thai. Dữ liệu dược động học lâm sàng của pyronaridine cho thấy thời gian thải loại bán hủy (elimination T1/2 lần lượt là 13,2 và 9,6 ngày trên người lớn và trẻ em mắc SR cấp tính chưa biến chứng do P. falciparum và P. vivax khi dùng thuốc phối hợp có artemisinins. Các dữ liệu lâm sàng đối với liệu pháp dùng đơn trị liệu hoặc dùng phối hợp của pyronaridine cho thấy tác động tuyệt vời chống lại P. falciparum và các nghiên cứu thuốc phối hợp cũng cho thấy đầy hứa hẹn chống lại chủng Plasmodium vivax. Pyronaridine đã được phát triển dạng liều phối hợp trong cùng viên với thuốc artesunate với tỷ lệ 3:1 trong điều trị SR cấp chưa biến chứng do P. falciparum và các giai đoạn trong hồng cầu của P. vivax với tên thuốc thương mại Pyramax® và nhận được nhiều ý kiến tốt về loại thuốc này từ Cơ quan thuốc châu Âu (European Medicines Agency).
Một số nghiên cứu đánh giá hiệu lực của thuốc phối hợp có Pyronaridine + Artemisinines
Các bằng chứng đối với pyronaridine như một thuốc đi kèm (partner drug) trong điều trị SR kháng thuốc artemisinins trên mô hình động vật gặm nhấm (Philipp P. Henricha và cs., 2012). Sự gia tăng tại Đông Nam Á do chủng P. falciparum có tỷ lệ làm sạch KSTSR chậm, sau điều trị thuốc có dẫn chất artemisinins, cho thấy một nhu cầu xác định vai tò và hiệu lực của các thuốc ACTs hiện sẵn có phù hợp nhất để điều trị kháng artemisinin. Ở đây, các nhà nghiên cứu cho thấy rằng chủngPlasmodium berghei SANA trên gặm nhấm kháng thuốc artemisinin theo sau áp lực thuốc, đã được xác định nhờ vào sự làm sạch KST chậm và tái phát sớm sau khi cho liều cao artesunate hoặc chất chuyển hóa dihydroartemisinin. Sử dụng SANA và chủng nhạy N, các nhà nghiên cứu đã xem xét hoạt tính chống lại SR của 5 loại thuốc ACTs có tên là [artemether + lumefantrine], [artesunate + amodiaquine], [artesunate + mefloquine], [dihydroartemisinin+piperaquine] và thuốc phối hợp [artesunate + pyronaridine] này.
 |
Nhờ vào giám sát KSTSR trong máu và kết quả trong 30 ngày theo dõi kể từ khi liều đầu tiên chỉ định, cho thấy nhiễm trùng với chủng P. berghei SANA kháng artemisinin có thể điều trị thành công bằng thuốc phối hợp [artesunate + pyronaridine] mà ở nồng độ đó chữa khỏi chủng N. Không có thuốc đi kèm nào khác có hiệu quả ngang nhau trong việc điều trị nhiễm trùng SANA. Một trong 5 thuốc đi kèm được thử nghiệm, pyronaridine cũng cho hiệu quả nhất trong việc ức chế sự tái phát của ký sinh trùng SANA. Các dữ liệu này cho thấy tiềm năng lợi ích cho loại thuốc ACTs có thành phần pyronaridine trong vùng đã có SR kháng thuốc artemisinin.
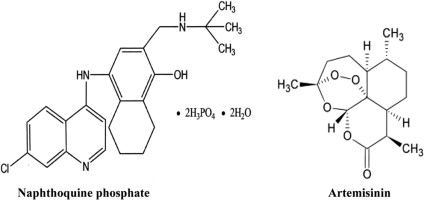
Về mặt dược lý học trên động vật, liệu pháp thuốc phối hợp ACTs này là sự phối hợp chứa naphthoquine phosphate và artemisinin với tỷ lệ 1:2,5. Chúng là một chất có hoạt tính diệt thể phân liệt mô giai đoạn hồng cầu các Plasmodium spp.
Hiệu lực thuốc phối hợp so với các thuốc artemisinin hoặc naphthoquine phosphate dùng đơn lẻ đã được nghiên cứu. Viên thuốc ARCO® đã phối hợp sự tác động nhanh trong diệt Plasmodium của artemisinin và một thuốc đi kèm có hiệu ứng tác dụng kéo dài của naphthoquine phosphate. Các nghiên cứu kháng chéo trên mô hình động vật đã chỉ ra phối hợp ARCO® này trì hoãn KST hình thành kháng thuốc mà hiện tượng này đã từng xảy ra đối với từng thành phần của thuốc dùng đơn lẻ.
Thử nghiệm đánh giá độc tính học 14 ngày cho thấy liều an toàn đối với chuột là 70mg/kg·ngày; liều an toàn đối với chó là 17,5mg/kg·ngày; cơ quan đích bị độc tính chính là gan và tủy xương. Các thông số dễ nhạy cảm bị tác động là men gan alanine aminotransferase (ALT), aspartate aminotransferase (AST) và tế bào hồng cầu lưới. Tất cả các thay đổi về mặt bệnh học có thể phục hồi sau khi dùng thuốc trên mô hình động vật. Cả naphthoquine phosphate và artemisinin đều hấp thu nhanh và phân bố vào trong ruột sau khi uống. Sau liều dùng liều duy nhất của ARCO® trước bữa ăn, Cmax của naphthoquine phosphate chỉ ra 1 giá trị 27.44µg·L, trong khi artemisinin có Cmax là 697.70µg·L. Chế độ ăn uống khi dùng viên ARCO® làm giảm sự hấp thu naphthoquine phosphate, giảm đến 47% AUC (diện tích dưới đường cong) và Cmax củanaphthoquine qua thời gian đói nên viên ARCO® nên uống trước khi ăn.
Naphthoquine phosphate gắn kết protein cao (89%) với ngưỡng nồng độ 11 - 44 µg·L-, Naphthoquine được phát hiện chủ yếu phân bố trong tạng thận, gan, phổi, não và lách. Tỷ lệ gắn proteine huyết tương của artemisinin là 64%. Artemisinin được phân bố rộng rãi và nồng độ cao hơn tìm thấy trong ruột, gan, mô não và thận. Hầu như naphthoquine phosphate vẫn giữ nguyên thể cho đến khi đào thải khỏi cơ thể, một số chất chuyển hóa gồm carboxylic acid và chất chuyển hóa không xác định.
Artemisinins chuyển hóa nhanh nhờ microsomes, với chất chuyển hóa chính của dihydroartemisinin. Chu trình oxy hóa khử của cytochrome P-450 cũng đã được mô tả.
Artemisinin chủ yếu đào thải qua thận và đường ruột trong vòng 24 giờ. Có 84% số này đào thải qua 24 giờ. Naphthoquine phosphate đào thải chủ yếu qua nước tiểu, chiếm 44% tổng số và chu trình gan ruột có liên quan đến vấn đề đào thải này. Chế độ ăn uống cùng với thời điểm dùng thuốc ARCO® làm tăng đào thải Naphthoquine phosphate đến 56% khi uống lúc đói, do vậy thuốc nên tránh dùng ngay sau bữa ăn.
Theo đường uống thuốc nên chỉ định liều dùng duy nhất đối với người lớn, 8 viên dùng một lần (tổng liều chứa Naphthoquine 400mg và artemisinin 1000mg). Một số tác dụng ngoại ý của thuốc đã được báo cáo.
Sau khi cho thuốc, 5% số bệnh nhân có biểu hiện buồn nôn và khó chịu dạ dày; một số bệnh nhân có tăng men gan thoáng qua ALT hay AST và các thông số này trở về bình thường sau khi dừng thuốc. Một số ít ca có biểu hiện chóng mặt.
Thuốc chổng chỉ định trên các bệnh nhân dị ứng với các thành phần của thuốc artemisinin và naphthoquine, các bệnh nhân suy gan hoặc thận nặng; các phụ nữ mang thai. Dùng thuốc thận trọng trên các bệnh nhân suy thận hoặc gan. Một liều lặp lại của ARCO® trong vòng 10 ngày không nên khuyến cáo do tích tụ thành phần Naphthoquine phosphate. Trên các bệnh nhân SR nặng hoặc nôn mửa liên tục, liệu pháp thuốc SR thay thế là cần thiết ngay.
Các thử nghiệm trên động vật dùng liều cao, các dẫn chất artemisinin có ảnh hưởng về mặt gây quái thai lên phôi thai, trong khi không có ảnh hưởng lên thai nhi giai đoạn sau (sau 6 tháng). Naphthoquine phosphate không gây quái thai và không gây độc tính trên sinh sản trên mô hình chuột thử nghiệm. ARCO® sẽ được dùng nếu lợi ích lớn hơn nguy cơ cho thai nhi. Thuốc vẫn sử dụng trên các phụ nữ mang thai hơn 6 tháng. Chỉ có một lượng nhỏ thuốc artemisinin vànaphthoquine được đào thải vào trong sữa. Không có tác động dược lý học nào trên bà mẹ có liên quan đến viên thuốc ARCO® được phát hiện trên các trẻ em nhỏ khi các bà mẹ sử dụng thuốc. Tuy nhiên, thuốc nên sử dụng thận trọng trên các bà mẹ đang cho con bú.
Viên thuốc ARCO® là một dạng công thức thuốc phối hợp, chứa artemisinin tác động nhanh và thành phần Naphthoquine phosphate cho hiệu quả kéo dài. Thuốc phối hợp này có 2 thành phần cho tác dụng cộng hưởng (synergistic effect). Chỉ số cộng lực hay động vận (synergistic index) là 8.2 đối với các chủng Plasmodium kháng chloroquine trên mô hình động vật. Không thấy tác dụng ngoại ý nào tìm thấy khi viên ARCO® dùng đồng thời với thuốc paracetamol, thuốc kháng viên không steroides, các vitamin, thức ăn bổ sung và thuốc an thần kinh hoặc kháng sinh.
Chưa biết một antidote nào đối với artemisinins và naphthoquine phosphate. Liều vượt quá 50% liều khuyến cáo vẫn còn xem là liều an toàn. Giảm bạch cầu hạt thoáng qua và có thể phục hồi lại bình thường có thể nhìn thấy trong công thức máu trên các bệnh nhân nếu dùng quá liều 100%liều khuyến cáo, liều đến 1200 mg naphthoquine đã được báo cáo. Tuy nhiên, các bệnh nhân cần điều trị theo dõi tại bệnh viện nếu một khi tổng liều vượt quá 150% liều khuyến cáo. Các chỉ số cận lâm sàng như ALT, AST, alkaline phosphatase (ALP) và bạch cầu hạt nên giám sát cẩn trọng một khi dùng quá liều.
Hiệu lực [Artemisinin-Naphthoquine] điều trị SR P. falciparum và P. vivax chưa biến chứng
Một bản tổng quan về thuốc Artemisinin-Naphthoquine (ARCO®) do nhóm tác giả Francis W. Hombhanje, Qingyun Huang thực hiện (2013) cho thấy với sự lan rộng nhanh chóng của P. falciparum kháng với các thuốc không phải artemisinins sẵn có thì nhu cầu một thuốc mới rất cần thiết. ARCO® là một thế hệ mới của nhóm thuốc phối hợp có gốc artemisins ACTs, xuất phát từ hai loại thuốc chống sốt rét độc lập gồm artemisinin và naphthoquine phosphate, phối hợp lại với nhau hình thành loại artemisinin-naphthoquine.
Cả thuốc artemisinin và naphthoquine đều chứng minh có hiệu lực, an toàn và dung nạp tốt khi dùng đơn trị liệu. Thuốc phối hợp artemisinin-naphthoquine mang lại một lợi điểm mới mà các ACTs khác đang tồn tại: nó có thể chỉ định liều 1 ngày duy nhất đường uống. Một số nghiên cứu điều trị tiến hành gần đây cho thấy liều dùng đường uống liều duy nhất artemisinin-naphthoquine có hiệu quả tương đương liệu trình 3 ngày của thuốc artemether-lumefantrine và các loại ACTs. Điều này sẽ thể hiện cho ARCO® như một thế hệ mới của ACTs trong điều trị sốt rét chưa biến chứng do P. falciparum.
Một nghiên cứu dược động học tiến hành dùng thuốc phối hợp Artemisinin-naphthoquine trong điều trị sốt rét chưa biến chứng do P. falciparum Batty KT và cs., 2012) cho thấy artemisinin-naphthoquine (ART-NQ) là một liệu pháp chống sốt rét theo công thức phối hợp liều duy nhất thực hiện tại Papua New Guinea và một số quốc gia vùng nhiệt đới khác. Để đánh giá về đặc tính dược động học của các thành phần thuốc, đặc biệt là tetra-aminoquinoline NQ, nhóm nghiên cứu đã đi sâu vào nghiên cứu sự phân bố của ART-NQ trên các trẻ em tuổi từ 5 -12 củaPapua New Guinea mắc sốt rét chưa biến chứng, so sánh với liều duy nhất (15 và 6 mg/kg cân nặng) uống cùng với nước (nhóm 1; n = 13), liều duy nhất (22 và 9 mg/kg) uống cùng với sữa (nhóm 2; n = 17) và liều hai lần mỗi ngày 22 và 9 mg/kg với nước (nhóm 3; n = 16).
Nồng độ NQ trong huyết tương được đánh giá bằng hệ thống sắc ký lỏng cao áp và nồng độ ART trong huyết tương được kiểm tra bằng hệ thống sắc ký khối phổ. Mô hình dược động học đa phần dựa trên quần thể đối với NQ và ART được phát triển. Sự phân bố NQ đăc trưng tốt nhất bởi một mô hình 3 khoang với chỉ số thời gian bán hủy hấp thu trung bình (t(1/2)) là 1 giờ và nồng độ trong huyết tương tối đa trung bình tiên đoán là cao 57 μg/L sau liều thứ hai của nhóm 3. Thông số thời gian bán hủy đào thải trung bình của NQ t(1/2) là 22,8 ngày; làm sạch tương đối so với sinh khả dụng (CL/F) là 1,1 liters/giờ/kg; thể tích tại tình trạng tĩnh so với sinh khả dụng (V(ss)/F) là 710 l/kg. Chỉ định NQ với bữa ăn có chất béo (8.5 g; 615 kJ) so với nước có liên quan làm gia tăng sinh khả dụng 25%. Sự phân bố ART biểu hiện rõ nét bởi một mô hình hai khoang với chỉ số CL/F trung bình (4.1 l/giờ/kg) và V/F (21 l/kg) tương tự như các nghiên cusu trước đây. Giảm 77% về sinh khả dụng trong nhóm 3 ở liều sử dụng thứ 2 của ART. Thuốc NQ có các đặc tính dược động học mà cho phép xác định tiềm năng của nó như một thuốc đi cùng với artemisinin trong điều trị SR chưa biến chứng trên trẻ em.
Một nghiên cứu đánh giá hiệu lực thuốc phối hợp [Artemisinin-naphthoquine] so với chloroquine-primaquine trong điều trị sốt rét do P. vivax qua một nghiên cứu lâm sàng ngẫu nhiên có đối chứng tại tỉnh Yunnan, Trung Quốc (Hui Liu và cs., 2013) cho biết P. vivax là một loài KSTSR chính ở Trung Quốc và Trung Quốc đang nổ lực tiến đến loại trừ SR vào năm 2020.tỷ lệ chữa khỏi của P. vivax là một trong những thách thức trong chiến lược loại trừ SR. Mục đích của nghiên cứu là đánh giá hiệu lực và tính an toàn của phối hợ artemisinin-naphthoquine (ANQ) so với chloroquine-primaquine (CQ - PQ) trong điều trị P. vivax tại tỉnh Yunnan, Trung Quốc. Một nghiên cứu thiết kế không thấp kém hơn (non-inferiority) và ngẫu nhiên mở, các bệnh nhân đủ tiêu chuẩn nhiễm đơn thuần P. vivax được chọn ngẫu nhiên nhận một trong hai phác đồ thuốc hoặc là ANQ 24,5 mg/kg (naphthoquine 7 mg/kg và artemisinin 17,5 mg/kg), một lần một ngày trong 3 ngày, hoặc tổng liều CQ là 24 mg base/kg, một lần mỗi ngày trong 3 ngày kèm theo liều PQ là 0,45 mg base/kg/ngày, một lần mỗi ngày trong 8 ngày. Các bệnh nhân được theo dõi 1 năm. Sự khác biệt về hiệu lực giữa ANQ và CQ-PQ được so sánh thông qua Wilsontest.
Kết quả cho thấy vào ngày D42, số bệnh nhân không tái phát là 125 (98,4%; 95% CI,94,4 – 99,8%) đối với nhóm thuốc ANQ và 123 (96,1%; 95%CI, 91,1 – 98,7%) đối với CQ - PQ,và không có ý nghĩa thống kê (P = 0,4496). Vào ngày 365, số bệnh nhân là 101 (79,5%; 95%CI, 71,8 – 85,9%) đối với ANQ và 106 (82,8%; 95%CI, 75,1 – 88,9%) đối với CQ - PQ và không có ý nghĩa thống kê (P = 0,610). Vì thể tỷ lệ bệnh nhân không tái phát không có sự khác biệt giữa nhóm ANQ và CQ - PQ vào ngày D28, 42 và 365; so với CQ - PQ, tác dụng ngoại ý của ANQ nhẹ. Nhìn chung, thuốc NQ không kém hơn so với CQ-PQ trong điều trị các bệnh nhân để tránh tái phát và an toàn hơn CQ - PQ.
Thuốc phối hợp Artemisinin-naphthoquine (ARCO®) dùng điều trị các bệnh nhân SR chưa biến chứng do P. falciparum người lớn ở Papua New Guinea qua một nghiên cứ báo cáo về độ an toàn và hiệu lực (Francis W Hombhanje và cs., 2009). Việc sử dụng thuốc SR phối hợp có artemisinin hay với một dẫn suất của nó giờ đây đang được sử dụng rộng rãi và khuyến cáo dùng để khắc phục tình trạng P. falciparum kháng thuốc cũng như P. vivax.
Liệu trình thuốc phối hợp đường uống loại artemisinin-naphthoquine (ANQ, ARCO®) là một loại thuốc ACTs mới đang được tiếp tục đánh giá về mặt lâm sàng. Một nghiên cứu tiến hành để đánh giá về tính an toàn, hiệu lực và tính dung nạp với thuốc ANQ trong một vùng đa kháng thuốc để ghi nhận dữ liệu cơ bản trên quần thể bệnh nhân người lớn tại Papua New Guinea.
Đánh giá thử nghiệm lâm sàng thiết kế theo nghiên cứu ngẫu nhiên mở hai nhánh (two-arm) so sánh thuốc ANQ liệu trình liều duy nhất và liệu trình ba ngày của (10 mg/kg/ngày) chloroquine với sulphadoxine-pyrimethamine (CQ + SP) để điều trị SR do P. falciparum chưa biến chứng theo quy trình theo dõi 28 ngày trên quần thể bệnh nhân người lớn. Đánh giá kết quả đầu tiên về hiệu lực chữa khỏi vào ngày D1, 2, 3 7, 14 và D28. Đánh giá kết quả sau đó gồm có thời gian làm sạch KSTSR, thời gian cắt sốt và người mang giao bào. Đo lường kết quả chính về tính an toàn sau điều trị về mặt lâm sàng và cận lâm sàng.
Từ 2005-2006, tổng số 130 bệnh nhân SR do P. falciparum được chọn đưa vào ngẫu nhiên dùng thuốc ANQ và CQ + SP, chỉ có 100 bệnh nhân (51 bệnh nhân ở nhóm ANQ và 49 bệnh nhân nhóm (CQ + SP) được đánh giá về mặt lâm sàng và ký sinh trùng.
Tất cả bệnh nhân được điều trị bằng thuốc ANQ và CQ + SP cho thấy đáp ứng về mặt lâm sàng và ký sinh trùng đầy đủ theo dõi qua 28 ngày. Tỷ lệ chữa khỏi đối với nhóm dùng ANQ vào ngày D1, 2, 3, 7, 14, vàD28 lần lượt là 47%, 86%, 92%, 94%, 94% và 94%. Sự tái phát chiếm 6%; tất cả đều sạch ký sinh trùng vào ngày D21. Đối với nhóm dùng CQ + SP tỷ lệ chữa khỏi lần lượt là 24%, 67%, 82%, 82%, 84% và 88%. Tỷ lệ tái phát là 10%, tất cả đều sạch KST vào ngày D28, ngoại trừ 1 bệnh nhân.
Cả hai phác đồ đều dung nạp thuốc tốt, không thấy tác dụng ngoại ý nghiêm trọng. Tỷ lệ người mang giao bào cao hơn ở nhóm dùng CQ + SP so với nhóm dùng ANQ (41% so với 12%; p < 0,05). Trong khi các dữ liệu này chưa đầy đủ, nhưng các bằng chứng trên cũng đã cho thấy thuốc phối hợp ANQ liều duy nhất rất an toàn và hiệu quả cao trong điều trị SR chưa biến chứng do P. falciparum trên quần thể người lớn Papua New Guinea và cần có những nghiên cứu thêm.
Nghiên cứu về hiệu lực và tính an toàn của thuốc phối hợp artemisinin-naphthoquine (AN) so với dihydroartemisinin-piperaquine (DHA - PPQ) trên các bệnh nhân trưởng thành mắc SR chưa biến chứng qua một thử nghiệm đa trung tâm tại Indonesia (Emiliana Tjitra và cs., 2012) cho thấy một liệu pháp mang tính thực hành và đơn giản cho điều trị các loài nhằm hướng đến loại trừ SR ở Indonesia.
Điều quan trọng là so sánh hiệu lực và tính an toàn của liều duy nhất của artemisinin-naphthoquine (AN) với liệu trình 3 ngày của dihydroartemisinin-piperaquine (DHP) là loại thuốc đang dùng trong chương trình, đối với các bệnh nhân trưởng thành mắc SR không biến chứng. Nghiên cứu này là thử nghiệm pha III tại đa trung tâm Jayapura và Maumere. Tiểu chuẩn chọn bệnh nhân theo TCYTTG có cải tiến đẻ đánh giá trong thử nghiệm.
Tổng số 401 bệnh nhân đủ tiêu chuẩn nhập viện trong ba ngày và chia ra điều trị ngẫu nhiên hoặc AN 4 viên liều duy nhất vào ngày D0 hoặc DHA-PPQ liệu trình 3 ngày liên tiếp. Theo dõi 42 ngày và khám lâm sàng làm lam máu giọt dày và giọt mỏng và một số xét nghiệm khác cần thiết. Hiệu lực của thuốc được đánh giá có hiệu chỉnh bằng PCR.
Kết quả cho thấy có 153 ca P. falciparum, 158 ca P. vivax và 90 P. falciparum/ P. vivax. Thời gian cắt sốt trung bình là tương đương nhau, 13,0±10,3 giờ ở nhóm AN và11,3± 7,3 giờ ở nhóm dùng DHA-PPQ. Thời gian làm sạch KSTSR trung bình dài hơn ở nhóm AN so với nhóm DHA-PPQ (28,0 ±11,7 giờ so với 25,5 ± 12,2 giờ, p= 0,04).Chỉ có 12 ca thấy bại điều trị được hiệu chỉnh PCR (7 ca nhóm AN và 5 ca nhóm DHA-PPQ).
Đáp ứng lâm sàng và KST đầy đủ chưa hiệu chỉnh và hiệu chỉnh PCR vào ngày thứ 42 là 93,7% (95% Cl: 90,3 – 97,2) và 96,3% (95% Cl: 93,6 – 99,0) trên nhóm AN, 96,3% (95% Cl: 93,5 – 99,0) và 97,3% (95% Cl: 95,0 – 99,6) trên nhóm dùng DHA - PPQ. Một só tác dụng ngoại ý được báo cáo. Các thông số sinh hóa và huyết học lâm sàng không bất thường. Kết luận cho thấy cả thuốc AN và DHA - PPQ được xác định rất hiệu quả, an toàn và dung nạp thuốc tốt trong điều trị SR và cả hai thuốc đều hứa hẹn là thuốc lựa chọn trong chính sách thuốc ưu tiên tại Indonesia.
Một nghiên cứu trên mô hình động vật để đánh giá tác động thuốc AN lên các thông số sinh hóa của các con chuột nhiễm KSTSR P. berghei (Onasanya S Sunday và cs., 2012).Tổng số 7 nhóm của 15 con chuột Albino được gây nhiễm chuẩn (1x 107 ) trong phúc mạc với P. berghei:
+ Nhóm 1 (chứng) gây nhiễm nhưng không điều trị,
+ Nhóm 2 gây nhiễm và được điều trị bằng thuốc chloroquine (10mg/kg) trong 3 ngày.
+ Nhóm 3 gây nhiễm và điều trị bằng thuốc artesunate (ART) 4mg/kg trong 3 ngày.
+ Nhóm thứ 4 gây nhiễm và điều trị bằng thuốc Artemether-lumefantrine (A-L) 56 mg/kg, rồi sau 8 giờ, rồi đến 2 lần mỗi ngày trong hai ngày tiếp theo.
+ Nhóm 5 gây nhiễm và điều trị với thuốc dihydroartemisinin-piperaquine (18mg/kg trong 2 ngày và 12mg/kg trong ngày thứ 3). Nhóm 6 gây nhiễm và điều trị bằng Artemisinin-naphthoquine (ANQ), 23mg/kg một lần mỗi ngày chỉ trong một ngày. Nhóm 7 gây nhiễm và điều trị bàng artemisinin-naphthoquine (ANQ), 7,6mg/kg một lần mỗi ngày trong 3 ngày.
Tất cả thuốc được chỉ định đường uống, lấy máu qua canul đếm mật độ KSTSR và sau đó giám sát sự làm sạch KST. 24 giờ sau khi chỉ định thuốc, gan và thận của 4 con vật từ các nhóm điều trị khác nhau được loại bỏ sau khi chết và sử dụng để phân tích nồng độ malondialdehyde (MDA), hydrogen peroxide generation, superoxide dismutase (SOD), catalase (CAT), hoạt tính glutathione-S- transferase (GST) và glutathione giảm (GSH).
Kết quả cho thấy rằng, uống thuốc ANQ trong 3 ngày liên tiếp ở liều 7.3mg/kg cho sự khác biệt về làm sạch KST trên chuột vào ngày thứ 2 so với ANQ liều duy nhất, phục hồi PCV nhanh hơn liều duy nhất của ANQ, cho chỉ số tỷ lệ sống còn trung bình cao hơn so với nhóm ANQ dùng liều duy nhất. Tăng nồng độ CAT và SOD trong gan và thận trên các con chuột điều trị bằng liều ANQ duy nhất với sự khác biệt có ý nghĩa thống kê giữa ANQ 3CD và ANQ liều duy nhất xác định sự bảo vệ gan và thận của ANQ khi sử dụng liều cao.
Một nghiên cứu đánh giá hiệu lực và tinh an toàn của thuốc phối hợp artemisinin-naphthoquine phosphate đường uống trong điều trị SR do P. falciparum chưa biến chứng tiến hành tại Myanamr (Tun T và cs., 2009). Tất cả thuốc phối hợp ACTs, được khuyến cáo bởi TCYTTG là liệu trình 3 ngày. Một phiên bản đánh giá mức độ không phối hợp /hài lòng với liệu trình này đã báo cáo tại một số quốc gia. Nghiên cứu này nhằm mục đích đánh giá hiệu lực của liều duy nhất với thuốc thế hệ mới ACTs chứa artemisinin plus naphthoquine. Liệu trình liều duy nhất 8 viên (400 mg naphthoquine + 1000 mg artemisinin) của thuốc phối hợp chỉ định cho các bệnh nhân SR người lớn do P. falciparum. Đánh giá về mặt lâm sàng và cận lâm sàng cũng như xuất hiện lại KSTSR vào các ngày D0, 1, 2, 3, 7, 14, 21 và D28.
Tổng số 53 ca bệnh SR do P. falciparum dương tính có sốt hoặc tiền sử sốt trong vòng 24 giờ trước khi nghiên cứu. Thời gian cắt sốt trung bình (FCT), thời gian làm sạch KSTSr trung bình (PCT) lần lượt là 18,2 ± 8,6 giờ và 34,6 ± 14,3 giờ. Đáp ứng lâm sàng và KSTSR đầy đủ trên 52/53 ca (98,1%) (95% CI, 91.1 - 99.9). Một bệnh nhân được phân loại là thất bại ký sinh trùng muộn do xuất hiện lại KST loài P. falciparum vào ngày D14. Thuốc dung nạp tốt trên bệnh nhân và không có tác dụng ngoại ý nào trên các bệnh nhân. Vì liều dùng duy nhất, các nhân viên y tế có thể chỉ định và theo dõi trực tiếp cho bệnh nhân là có khả thi theo liệu trình điều trị có giám sát trực tiếp (DOTs).
Nhìn chung, thuốc phối hợp ACTs mới này sẽ là một trong những ứng cử viên trong điều trị SR do P. falciparum và P. vivax đa kháng thuốc trong tương lai khi mà các thế hệ ACTs khác đang dần dần có những thách thức và nguy cơ giảm nhạy và xuất hiện chủng kháng thuốc đối mặt hiện nay.
Tài liệu tham khảo
1.Batty KT, Salman S, Moore BR, Benjamin J, Lee ST, Page-Sharp M, Pitus N, Ilett KF, Mueller I, Hombhanje FW, Siba P, Davis TM (2012), Artemisinin-naphthoquine combination therapy for uncomplicated pediatric malaria: a pharmacokinetic study, Antimicrob Agents Chemother. 2012 May;56(5):2472-84.
2.Francis W Hombhanje,David Linge, Adolf Saweri, Cynthia Kuanch, Robert Jones, Stephen Toraso, Jacobed Geita, Andrew Masta, Isi Kevau, Gilbert Hiawalyerand Mathias Sapuri (2009), Artemisinin-naphthoquine combination (ARCO™) therapy for uncomplicated falciparum malaria in adults of Papua New Guinea: A preliminary report on safety and efficacy, Malaria Journal 2009, 8:196
3.Francis W. Hombhanje, Qingyun Huang (2013), Artemisinin-Naphthoquine Combination (ARCO®): An Overview of the Progress, Special Issue New Antimalarial Drugs
4.Hui Liu, Heng-lin Yang, Jian-Wei Xu, Jia-zhi Wang, Ren-hua Nie, Chun-fu Li (2013), Artemisinin-naphthoquine combination versus chloroquine-primaquine to treat vivax malaria: an open-label randomized and non-inferiority trial in Yunnan Province, China, Malaria Journal 2013, 12:409.
5.Emiliana Tjitra, Armedy R Hasugian, Hadjar Siswantoro, Budi Prasetyorini, Riyanti Ekowatiningsih, Endah A Yusnita, Telly Purnamasari, Srilaning Driyah, Ervi Salwati, Nurhayati, Eni Yuwarni, Lidwina Januar, Joseph Labora, Bambang Wijayanto, Fajar Amansyah, Tersila AD Dedang, Asep Purnama, Trihono (2012), Efficacy and safety of artemisinin-naphthoquine versus dihydroartemisinin-piperaquine in adult patients with uncomplicated malaria: a multi-centre study in Indonesia, Malaria Journal 2012, 11:153.
6.Tun T., Tint H.S., Lin K., Kyaw T.T., Myint M.K., Khaing W., Tun Z.W (2009),Efficacy of oral single dose therapy with artemisinin-naphthoquine phosphate in uncomplicated falciparum malaria, Acta Trop. 2009 Sep !important;111(3):275-8.
7.Philipp P. Henricha, Connor O'Briena, Fabián E. Sáenzb, Serge Cremersc, Dennis E. Kyleb and David A. Fidocka (2014), Evidence for Pyronaridine as a Highly Effective Partner Drug for the Treatment of Artemisinin-Resistant Malaria in a Rodent Model, Antimicrob Agents Chemother. 2014 Jan;58(1):183-95.
8.Simon L Croft, Stephan Duparc, Sarah J Arbe-Barnes, J Carl Craft, Chang-Sik Shin, Lawrence Fleckenstein, Isabelle Borghini-Fuhrer and Han-Jong Rim (2012), Review of pyronaridine anti-malarial properties and product characteristics, Malaria Journal 2012, 11:270.
9.Henrich P.P., O'Brien C., Saenz F.E., Cremers S., Kyle D.E., Fidock D.A (2014), Evidence for pyronaridine as a highly effective partner drug for treatment of artemisinin-resistant malaria in a rodent model, Antimicrob Agents Chemother. 2014 Jan;58(1):183-95