Lây lan nhanh và tỷ lệ tử vong cao là sự kết hợp đặc biệt nguy hiểm của virus SARS-CoV-2, đây là loại virus gây ra bệnh COVID-19. Từ khi dịch bệnh COVID-19 xuất hiện, hệ thống y tế hiện đại khắp toàn cầu đã rơi vào tình trạng quá tải, hàng triệu bác sĩ, nhân viên y tế và người dân bị nhiễm bệnh. Vì vậy, để phòng tránh những mất mát khủng khiếp do COVID-19 gây ra, cùng với những biện pháp chẩn đoán, xét nghiệm, điều trị và phòng, chống dịch hiệu quả thì vắc-xin là công cụ quan trọng giúp kiểm soát đại dịch COVID-19.
Chính vì thế, việc tìm kiếm một loại vắc-xin an toàn và hiệu quả đề phòng ngừa nguy cơ nhiễm COVID-19 đang là vấn đề quan tâm hàng đầu hiện nay. Cho nên, việc cấp bách cần phải làm là thúc đẩy sản xuất vắc-xin và chia sẻ vắc-xin là vấn đề cực kỳ quan trọng được WHO lan tỏa nhằm chấm dứt đại dịch trên toàn cầu.
Trên thế giới, hiện nay có rất nhiều loại vắc-xin được các nước sản xuất với phương pháp tiếp cận riêng. Theo đó, mỗi một loại vắc-xin đều có mức độ an toàn và khả năng bảo vệ khác nhau trong việc phòng nhiễm vi rút SARS-CoV-2 có triệu chứng.
Kể từ tháng 12 năm 2020, vắc-xin COVID-19 đã bắt đầu được phân phát và sử dụng tại nhiều quốc gia trên thế giới. Ủy ban Tư vấn Toàn cầu về An toàn vắc-xin (Global Advisory Committee on VaccineSafety_GACVS)-là một nhóm các chuyên gia cung cấp hướng dẫn độc lập và có cơ sở khoa học chặt chẽ cho WHO về chủ đề sử dụng vắc-xin an toàn – đã nhận và đánh giá các báo cáo về sự cố an toàn nghi ngờ có khả năng gây ảnh hưởng quốc tế.
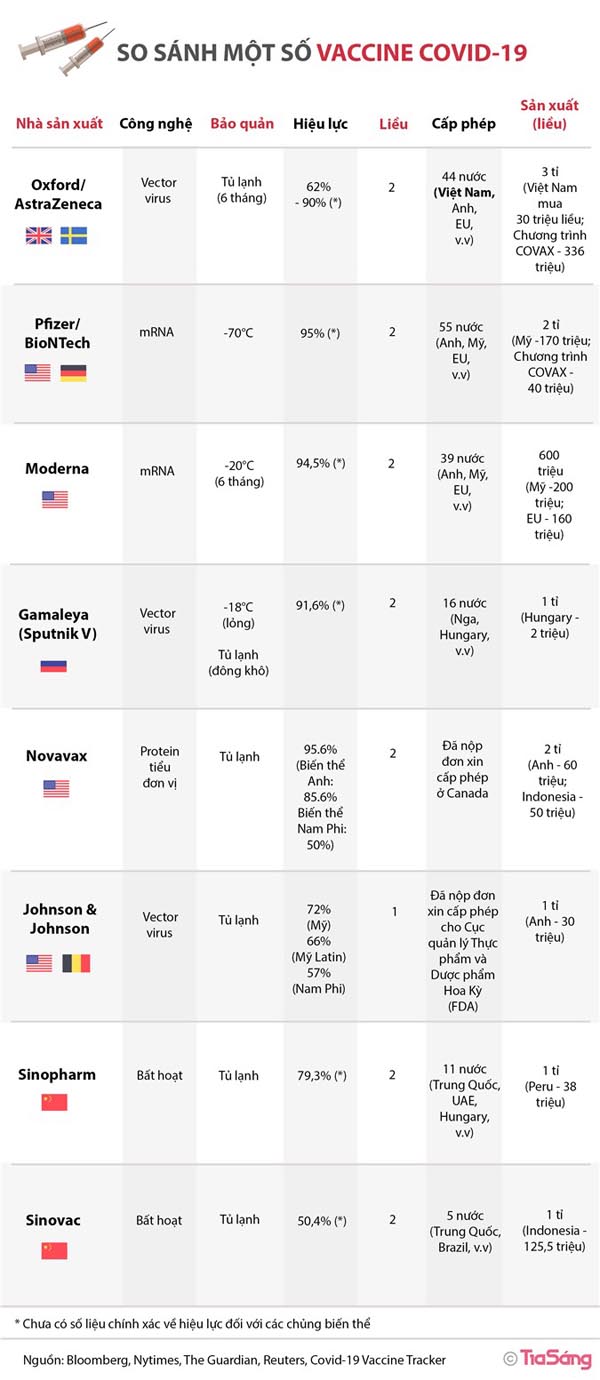
Tại Việt Nam, tính đến thời điểm hiện nay, có 6 loại vắc-xin phòng COVID-19 đã được Bộ Y tế cấp phép sử dụng gồm:vắc-xinCOVID-19 của Oxford/AstraZeneca; vắc-xin Gam-COVID-Vac (tên khác là SPUTNIK V); vắc-xin Vero Cell do Sinopharm; vắc-xin Comirnatycủa công ty Pfizer-BioNTech; vắc-xin Spikevax do Moderna sản xuất; vắc-xin Janssen do Janssen Pharmaceutica NV (Bỉ) và Janssen Biologics B.V (Hà Lan) sản xuất. Tất cả các loại vắc-xin này đều được đánh giá đảm bảo an toàn, hiệu quả [1].
1. Vắc-xin phòng COVID-19- Oxford/AstraZeneca
Vắc-xin phòng COVID-19 của AstraZeneca được đồng phát triển bởi Đại học Oxford và Hãng dược nổi tiếng thế giới-AstraZeneca (Vương quốc Anh) và đã được cấp phép sử dụng khẩn cấp tại 181 quốc gia, vùng lãnh thổ và được Tổ chức Y tế thế giới (WHO) đưa vào danh sách sử dụng khẩn cấp. Đến nay, vắc-xin này đã được sử dụng tại 119 quốc gia, vùng lãnh thổ với tổng số vắc-xin đã sử dụng khoảng 980 triệu liều.
Vắc xin COVID-19 của Oxford/AstraZeneca phòng chống COVID-19 có hiệu lực 63,09% trên những người nhiễm SARS-CoV-2 có triệu chứng. Khoảng cách giữa các liều dài hơn trong khoảng thời gian từ 8 đến 12 tuần có liên quan đến hiệu quả vắc xin cao hơn [3]. Đây là một con số vượt quá sự kỳ vọng của Tổ chức Y tế Thế giới (WHO), khi WHO công bố hiệu lực bảo vệ trước COVID-19 của vắc-xin chỉ cần đạt trên 50% là đã có thể được sản xuất rộng rãi phục vụ nhu cầu phòng bệnh của người dân.
Vắc-xin phòng COVID-19 AstraZeneca được phát triển bởi hãng dược AstraZeneca và Đại học Oxford (Vương quốc Anh)
Phân tích chính của các thử nghiệm lâm sàng giai đoạn III từ Anh, Brazil và Nam Phi, mới được công bố trên tờ The Lancet, xác nhận COVID-19 vắc-xin AstraZeneca an toàn và hiệu quả trong việc ngăn ngừa COVID-19, không có trường hợp nặng hay nhập viện xảy ra sau 22 ngày sau liều đầu tiên.
Theo các dữ liệu nghiên cứu cho thấy, vắc-xin phòng COVID-19 của hãng AstraZeneca có hiệu quả chống lại hầu hết các chủng virus gây bệnh COVID-19, kể cả biến thể virus Delta mới hiện đang lưu hành tại Việt Nam [4]. Dữ liệu gần đây của Cơ quan Y tế Công cộng Anh (Public Health England-PHE) chứng minh, hai liều vắc-xin COVID-19 của AstraZeneca có hiệu quả 92% trong việc giảm số ca nhập viện do biến thể Delta và cho thấy không có trường hợp tử vong trong số những người được tiêm chủng. Mặc khác, vắc-xin AstraZeneca cũng đạt được hiệu quả cao đối với biến thể Alpha (B.1.1.7, còn được biết đến là biến thể Kent), giúp giảm 86% số ca nhập viện và không có trường hợp tử vong nào được báo cáo. Đối với những trường hợp có triệu chứng nhẹ, vắc-xin giảm nguy cơ mắc bệnh COVID-19 có triệu chứng là 74% với biến chủng Alpha và 64% đối với biến chủng Delta [4].
Bên cạnh đó, kết quả nghiên cứu lâm sàng của vắc-xin phòng COVID-19 của AstraZeneca cũng đã chứng minh được tính an toàn của loại vắc-xin này, khi không ghi nhận bất kỳ vấn đề sức khỏe nghiêm trọng nào. Theo hãng AstraZeneca, vắc-xin phòng COVID-19 của họ tạo ra phản ứng miễn dịch tốt, cũng như gây ít phản ứng phụ ở người lớn tuổi.
Trước đó, báo Financial Times (London, Anh) cũng đã công bố thông tin vắc-xin phòng COVID-19 của AstraZeneca có khả năng kích thích đáp ứng miễn dịch của tế bào lympho T và lympho B và sinh kháng thể bảo vệ ở nhóm người cao tuổi. Đây là kết quả rất đáng mừng, bởi tuổi càng cao khả năng miễn dịch của con người càng thấp. Trong khi đó, người cao tuổi lại là nhóm có nguy cơ mắc và tử vong cao do COVID-19. Hiệu quả của vắc-xin tiếp tục củng cố bằng chứng cho tính an toàn và khả năng miễn dịch của vắc-xin đối với cơ thể người.
Tại Việt Nam, vắc-xin AstraZeneca đã được Bộ Y tế phê duyệt có điều kiện cho nhu cầu cấp bách trong phòng, chống dịch COVID-19. Vắc-xin AstraZeneca được triển khai tiêm chủng tại Việt Nam từ tháng 3/2021, hiện đang có số lượng sử dụng nhiều nhất tại Việt Nam. Hiện nay, vắc-xin phòng COVID-19 của AstraZeneca được chỉ định tiêm chủng cho người từ 18 tuổi trở lên. Các nhà khoa học hiện đang tiếp tục tiến hành các cuộc thử nghiệm tiêm vắc-xin cho các đối tượng nhỏ hơn 18 tuổi.
Mới đây, Bộ Y tế cũng đã chính thức có hướng dẫn tiêm vắc-xin phòng COVID-19 cho người trên 65 tuổi. Cụ thể, theo Hướng dẫn sửa đổi, bổ sung Hướng dẫn tạm thời khám sàng lọc trước tiêm chủng vắc-xin phòng COVID-19 do Bộ Y tế ban hành ngày 15/7, người trên 65 tuổi trở lên thuộc nhóm đối tượng phải chuyển tiêm chủng và theo dõi tại bệnh viện.
Các chuyên gia y tế lưu ý rằng, người trên 65 tuổi, người có tiền sử bệnh nền, bệnh mạn tính được điều trị ổn định; tiền sử rối loạn đông máu/cầm máu hoặc đang dùng thuốc chống đông cần thận trọng tiêm chủng có chỉ định của bác sĩ và phải thực hiện tại khối bệnh viện hoặc các cơ sở y tế có năng lực, điều kiện xử trí tốt.
2. Vắc-xin Gam-COVID-Vac (tên khác là SPUTNIK V)
Vắc-xin Gam-COVID-Vac ( hay được gọi là vắc-xin Sputnik V) do Viện Nghiên cứu Gamaleya, Nga sản xuất đã được cấp phép sử dụng tại 70 quốc gia, vùng lãnh thổ. Đến nay, vắc-xin này đã được sử dụng tại 49 quốc gia với tổng số vắc-xin đã sử dụng khoảng 85 triệu liều.
Vắc-xin Gam-COVID-Vac (tên khác là SPUTNIK V)
Vắc-xin Sputnik V có hiệu quả bảo vệ khỏi COVID-19 đạt khoảng 91,6%, sản phẩm đáp ứng đầy đủ các quy chuẩn an toàn, giảm tỷ lệ mắc bệnh, tỷ lệ biến chứng và tử vong gây ra do Virus Corona gây ra. Vắc-xin này dựa trên nền tảng vector adenovirus- là một trong những loại vector được sử dụng nhiều nhất trong công nghệ gen, được đăng ký đầu tiên trên thế giới.Vector adenovirus là công nghệ mới và đa năng, cho hiệu suất sản xuất cao, không phụ thuộc vào việc nuôi cấy toàn thể tác nhân gây bệnh. Hiện nay, các nhà phát triển vắc-xin trên thế giới cũng đang tập trung vào công nghệ vector adenovirus để sớm có được vắc-xin COVID-19 phòng đại dịch [5].
Để đảm bảo khả năng miễn dịch lâu dài, các nhà khoa học Nga đã đưa ra một ý tưởng đột phá là sử dụng hai loại vector adenovirus khác nhau (rAd26 và rAd5) cho lần tiêm chủng thứ nhất và thứ hai. Người sử dụng vắc-xin Sputnik V sẽ phải tiêm 2 mũi, sử dụng hai loại vector khác nhau là rAd5 và rAd26. Bằng cách này, chúng sẽ “đánh lừa” cơ thể, kích thích miễn dịch đối với vector đầu tiên và tăng hiệu quả của vắc-xin với mũi thứ hai sử dụng vector khác.
Sputnik V của Nga thực chất là hai loại vắc-xin khác nhau, được tiêm cách nhau 21 ngày. Liều thứ nhất sử dụng vector là virus rAd26 (cùng loại với vắc-xin đang được phát triển bởi Johnson & Johnson và Trường Y Harvard). Liều thứ hai là các vector rAd5 (cùng loại với vắc xin đang được CanSino Biology phát triển ở Trung Quốc).Các nhà khoa học Nga cho rằng, việc tiêm một vắc-xin thứ hai khác mũi một sau 21 ngày sẽ giúp hệ miễn dịch củng cố khả năng nhận diện và chống lại virus SARS-CoV-2. Đồng thời, điều này được hy vọng là sẽ kéo dài khả năng miễn dịch hơn so với chỉ tiêm một liều một loại vắc xin hoặc 2 liều cùng một loại vắc-xin [5].
Tại Việt Nam, vắc-xin Sputnik V đã được Bộ Y tế phê duyệt có điều kiện vắc-xin cho nhu cầu cấp bách trong phòng, chống dịch COVID-19.
3. Vắc-xin Vero Cell của Sinopharm
Vắc-xin Vero Cell do Sinopharm phát triển và Beijing Institute of Biological Products Co., Ltd.,- Trung Quốc sản xuất, đã được cấp phép sử dụng tại 64 quốc gia, vùng lãnh thổ, đã được Tổ chức Y tế thế giới đưa vào danh sách sử dụng khẩn cấp. Đến nay, vắc-xin này đang sử dụng tại 59 quốc gia với khoảng 800 triệu liều đã được sử dụng.

Vắc xin Vero Cell của Sinopharm
Một thử nghiệm Giai đoạn 3 đa quốc gia cho thấy, sau 14 ngày kể từ khi tiêm đủ hai liều (khoảng cách giữa hai liều là 21 ngày) vắc xin có hiệu quả 79% phòng lây nhiễm vi rút SARS-CoV-2 có triệu chứng. Hiệu quả trong việc phòng ngừa nhập viện là 79% [6].
Thử nghiệm này không được thiết kế và có hiệu lực để chứng minh hiệu quả phòng ngừa bệnh nặng ở những người có bệnh nền, những người trong thời kỳ mang thai, hay những người từ 60 tuổi trở lên. Có ít đối tượng là phụ nữ tham gia vào nghiên cứu. Thời gian theo dõi trung vị ở thời điểm đánh giá dữ liệu là 112 ngày.
Có hai thử nghiệm đánh giá hiệu lực của vắc xin đang được triển khai nhưng chưa có số liệu.
Hiện nay, SAGE khuyến cáo sử dụng vắc xin này theo Lộ trình Ưu tiên của WHO.Khi có thêm số liệu mới WHO sẽ cập nhật các khuyến cáo. Vắc xin này vẫn chưa được đánh giá trong bối cảnh các biến thể mới đang lưu hành rộng rãi. Và không có nhiều số liệu về tác động của vắc xin COVID-19 BIBP đối với việc lây truyền vi rút SARS-CoV-2, loại vi rút gây bệnh COVID-19.
Tại Việt Nam, vắc-xin Vero Cell đã được Bộ Y tế phê duyệt có điều kiện cho nhu cầu cấp bách trong phòng, chống dịch COVID-19.
4. Vắc-xin phòng COVID-19 của công ty Pfizer BioNTech (BNT162b2)
WHO đã cấp phép EUL cho vắc-xin của Pfizer BioNTech vào ngày 31 tháng 12 năm 2020. WHO đã đánh giá kĩ lưỡng chất lượng, sự an toàn và hiệu lực của loại vắc-xin này và khuyến cáo sử dụng cho người trên 16 tuổi. Hiệu lực bảo vệ của vắc-xin bắt đầu 12 ngày sau liều đầu tiên nhưng để bảo vệ đầy đủ cần phải tiêm 2 liều theo khuyến cáo của WHO, khoảng cách giữa hai mũi tiêm là 21 – 28 ngày. Cần nghiên cứu thêm để hiểu hơn về khả năng bảo vệ tiềm năng lâu dài sau một liều đơn. Hiện tại, khuyến cáo sử dụng cùng loại sản phẩm cho cả hai liều.
Vắc-xin Comirnaty của Pfizer/BioNTech
Vắc-xinComirnaty của Pfizer/BioNTech đã được cấp phép sử dụng tại 111 quốc gia và vùng lãnh thổ và được Tổ chức Y tế thế giới đưa vào danh sách sử dụng khẩn cấp. Đến nay, vắc-xin này đã được sử dụng tại 97 quốc gia với khoảng 850 triệu liều đã được sử dụng và đã được Bộ Y tế phê duyệt có điều kiện cho nhu cầu cấp bách trong phòng, chống dịch COVID-19 tại Việt Nam.
Nhóm Chuyên gia Tư vấn Chiến lược về Tiêm chủng (Strategic Advisory Group of Experts on Immunization-SAGE) của WHO đã ra khuyến nghị chính sách về triển khai diện rộng vắc-xin COVID-19 đầu tiên được phê duyệt cho sử dụng khẩn cấp-vắc-xin COIVID-19 của công ty Pfizer-BioNTech.Theo SAGE, vắc-xin COVID-19 mRNA của Pfizer-BioNTech an toàn và hiệu quả. Ưu tiên tiêm chủng cho nhân viên y tế có nguy cơ phơi nhiễm cao trước, sau đó là người cao tuổi trước khi tiêm đại trà cho các nhóm còn lại.
Mặc khác, vắc-xin này cho thấy độ an toàn và hiệu quả ở những người có nhiều bệnh lý nền liên quan tới việc tăng nguy cơ mắc bệnh nặng.Các bệnh nền bao gồm tăng huyết áp, đái tháo đường, hen phế quản, bệnh phổi, gan hoặc thận cũng như các bệnh truyền nhiễm mạn tính đã ổn định và được kiểm soát. Mặc khác, hiệu quả vắc-xin được đánh giá là tương tự trên đối tượng phụ nữ đang trong thời kỳ cho con bú như với người trưởng thành khác.
Đối với thử nghiệm giai đoạn 3 ở trẻ 12 - 15 tuổi cho thấy vắc-xin có hiệu lực cao và an toàn ở nhóm tuổi này, do đó đã mở rộng chỉ định độ tuổi trước đây từ 16 tuổi trở lên thành từ 12 tuổi trở lên.Bằng chứng cho thấy trẻ vị thành niên, đặc biệt là nhóm lớn tuổi hơn, cũng có nguy cơ làm lây nhiễm SARS-CoV-2 như người trưởng thành. WHO khuyến cáo các nước cần cân nhắc việc sử dụng vắc-xin ở trẻ 12 – 15 tuổi chỉ khi đạt được tỷ lệ cao tiêm chủng vắc-xin đủ 2 liều ở các nhóm ưu tiên cao theo Lộ trình Ưu tiên của WHO. Trẻ từ 12 đến 15 tuổi mắc các bệnh đi kèm khiến trẻ có nguy cơ cao hơn đáng kể mắc COVID-19 nặng, cùng với các nhóm nguy cơ cao khác, có thể cần được tiêm chủng [7].
Các nghiên cứu cho thấy có tác động cao về y tế công cộng khi khoảng cách giữa các mũi tiêm dài hơn khoảng cách do EUL khuyến cáo. Theo đó, các nước có tỷ lệ mắc COVID-19 cao và thiếu hụt trầm trọng cung ứng vắc-xin có thể cân nhắc trì hoãn liều 2 tới 12 tuần để đạt được tỷ lệ bao phủ tiêm mũi đầu cao hơn ở các nhóm ưu tiên cao.
Vắc-xin Pfizer BioNTech phòng COVID-19 có hiệu lực 95% trong việc phòng nhiễm vi rút SARS-CoV-2 có triệu chứng [7]. SAGE đã rà soát lại tất cả số liệu hiện có về hiệu lực của vắc-xin này trong các thử nghiệm để đánh giá hiệu lực của chúng đối với các biến thể mới. Các thử nghiệm này cho thấy vắc-xin này hiệu quả với các biến thể mới.Hiện tại SAGE khuyến cáo sử dụng vắc-xin Pfizer BioNTech theo Lộ trình Ưu tiên của WHO, thậm chí nếu biến thể mới của vi rút xuất hiện trong nước. Khi các quốc gia đánh giá nguy cơ và lợi ích, cần cân nhắc tình hình dịch tễ của địa phương.
Các phát hiện ban đầu cho thấy nhu cầu cấp thiết là phải có sự phối hợp chặt chẽ trong giám sát và đánh giá các biến thể cũng như tác động tiềm năng của chúng đối với hiệu quả vắc-xin.
Ngày 23/8, Vắc-xin COVID-19 với hai mũi tiêm của Pfizer đã được Cơ quan Quản lý Thực phẩm và Dược phẩm Hoa Kỳ (FDA) phê chuẩn đầy đủ, và trở thành loại vaccine đầu tiên được cấp phép tại nước này. Theo báo New York Times, vắc xin do Pfizer/BioNTech nhận được giấy phép đầy đủ để sử dụng cho người từ 16 tuổi trở lên.
FDA đã cho phép Vắc xin Pfizer-BioNTech COVID-19 được sử dụng trong trường hợp khẩn cấp để ngăn ngừa COVID-19 ở người từ 12-15 tuổi trở lên. Trung Tâm Kiểm Soát và Phòng Ngừa Dịch Bệnh (CDC) khuyến nghị tiêm chủng COVID-19 cho tất cả mọi người từ 12 tuổi trở lên[8].
5. Vắc-xin Spikevax (Tên khác là: COVID-19 vắc-xin Moderna)
Vắc-xin Moderna (còn có tên khác là Skipevax hay mRNA-1273) là loại vắc-xin phòng COVID-19 được sản xuất theo công nghệ mới sử dụng vật chất di truyền RNA cho hiệu quả phòng bệnh lên tới 94,1% trong việc phòng ngừa lây nhiễm COVID-19 đã được phòng thí nghiệm xác nhận ở những người đã tiêm hai liều và không có bằng chứng bị nhiễm bệnh trước đó[9].
Vắc-xin Spikevax do Moderna sản xuất đã được cấp phép sử dụng tại 64 quốc gia, vùng lãnh thổ và được Tổ chức Y tế thế giới đưa vào danh sách sử dụng khẩn cấp. Đến nay, vắc-xin này đã được sử dụng tại 63 quốc gia với khoảng 340 triệu liều.
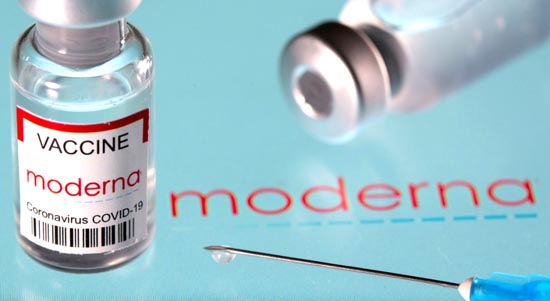
COVID-19 Vắc-xin Moderna
Để sản xuất vắc-xin mRNA-1273, các nhà khoa học Moderna đã nghiên cứu và dựa trên công nghệ dùng vật liệu di truyền (nucleic acid) gọi là mã RNA thông tin (mRNA). Hiện nay trên thế giới, chỉ có 2 hãng dược là Moderna và Pfizer (Mỹ) ứng dụng công nghệ này để bào chế vắc-xin COVID-19. Mặt khác, trước đây công nghệ mRNA đã được nghiên cứu cho bệnh cúm, sốt Zika, bệnh dại và virus cytomegalo (CMV).
Đối với vắc-xin mRNA, người tiêm sẽ nhận được vật liệu di truyền – mRNA (đây là vật liệu mã hóa protein virus). Khi vắc-xin mRNA được tiêm vào bắp tay, các tế bào cơ sẽ giải mã chúng để tạo ra protein virus trực tiếp trong cơ thể.
Cách tiếp cận này bắt chước những gì SARS-CoV-2 làm trong tự nhiên – nhưng mRNA của vắc-xin chỉ mã hóa cho đoạn quan trọng của protein virus. Điều này giúp cho hệ thống miễn dịch biết trước virus thật trông như thế nào mà không cần phải mắc bệnh. Đồng thời cũng giúp cho hệ thống miễn dịch có thời gian để tạo ra các kháng thể mạnh mẽ có thể vô hiệu hóa vi rút thật nếu người này bị nhiễm bệnh trong tương lai.
Trong trường hợp này, mRNA tổng hợp là vật chất di truyền, nó không thể được truyền cho thế hệ tiếp theo. Sau khi tiêm mRNA, phân tử này sẽ hướng dẫn các tế bào cơ sản xuất protein virus, nồng độ protein virus đạt đến mức cao nhất trong 24-48 giờ và có thể kéo dài vài ngày sau tiêm.
Điểm cộng khác cho dạng mRNA đó là có khả năng bền hơn trong việc chống lại mầm bệnh có xu hướng đột biến nhanh, chẳng hạn như virus SARS-CoV-2 hay virus cúm. Vắc-xin mRNA đã được chứng minh là “một sự thay thế đầy hứa hẹn” cho vắc xin truyền thống.
Theo các nhà khoa học, vắc-xin Moderna cho hiệu quả phòng COVID-19 lên đến 94,1%,một tỷ lệ thành công rất cao. Tiến sĩ Anthony Fauci, bác sĩ bệnh truyền nhiễm hàng đầu của quốc gia Hoa Kỳ cho biết: “Đây rõ ràng là những kết quả rất thú vị – 94,1% là thực sự xuất sắc”.Thêm vào đó, các nghiên cứu cho thấy vắc xin mRNA-1273 an toàn, dung nạp tốt, tạo ra phản ứng miễn dịch tốt trong cơ thể và không có tác dụng phụ quá nghiêm trọng.
Moderna là một trong số những công ty đầu tiên thử nghiệm vắc-xinCOVID-19 trên người, bắt đầu từ giữa tháng 3. Theo kết quả thử nghiệm lâm sàng giai đoạn cuối được Moderna công bố tháng 4/2021, vắc-xin cho hiệu quả phòng bệnh cao (94,1%), ngăn ngừa nguy cơ lây nhiễm, giảm tỷ lệ nhập viện và tử vong do bệnh.
Mặc dù vậy, theo FDA, vắc xin ít hiệu quả hơn ở người lớn tuổi, độ bảo vệ sẽ giảm xuống 86,4%. Trước đó, ngày 18/12,FDA của Mỹ đã phê duyệt cho phép sử dụng khẩn cấp (EUA) vắc-xin mRNA-1273 của Moderna, Mỹ chính thức sở hữu loại vắc xin thứ 2 đủ hiệu quả phòng ngừa COVID-19.
Đến ngày 6/1/2021, Cơ quan Dược phẩm Liên minh châu Âu (EMA) phê duyệt sử dụng khẩn cấp vắc-xinCOVID-19 do hãng dược Moderna điều chế đối với 27 quốc gia trong khối EU. Như vậy, các nước thuộc Liên minh châu Âu sẽ có loại vắc-xin thứ 2, sau vắc-xin Pfizer trong bối cảnh tỷ lệ lây nhiễm của châu Âu đang tăng mạnh, tốc độ tiêm chủng vẫn còn hạn chế.
Đặc biệt, vắc-xin Moderna đang được nghiên cứu chứng minh có hiệu quả trong việc chống lại các biến thể virus SARS-CoV-2 mới. Cụ thể, với biến chủng B.1.351 (Nam Phi) và ba biến chủng xuất hiện tại Ấn Độ, trong đó có chủng Delta, vắc-xin Moderna kích thích tạo ra kháng thể tồn tại trong cơ thể 6 tháng sau khi tiêm liều thứ 2. Những kháng thể này giúp cơ thể con người kháng lại virus SARS-CoV-2. Vì thế, vắc xin này được khuyên dùng vì có tính hiệu quả cao.
Vắc-xin này đã được Bộ Y tế phê duyệt sử dụng có điều kiện cho nhu cầu cấp bách trong phòng, chống dịch COVID-19.
6. COVID-19 Vắc-xin Janssen
Vắc-xin Janssen do Janssen Pharmaceutica NV (Bỉ) và Janssen Biologics B.V (Hà Lan) sản xuất được cấp phép sử dụng tại 56 quốc gia, vùng lãnh thổ và được Tổ chức Y tế thế giới đưa vào danh sách sử dụng khẩn cấp. Đến nay, vắc-xin này đã được sử dụng tại 34 quốc gia với khoảng 60 triệu liều đã sử dụng.
Vắc xin này sử dụng công nghệ virus vector, mỗi liều chứa 0,5ml và đặc biệt chỉ cần tiêm 1 mũi (các loại vắc xin trước đó nhập về Việt Nam tiêm 2 mũi), đối tượng tiêm chủng là từ 18 tuổi trở lên. Vắc-xin ngừa COVID-19 của J&J/Janssen đạt hiệu quả 66,3% trong các thử nghiệm lâm sàng (tính hiệu lực) phòng ngừa bệnh COVID-19 ở người đã chích vắc-xin và chưa có bằng chứng nhiễm bệnh trước đó. Mọi người có bảo vệ tốt nhất 2 tuần sau khi tiêm chủng [10]. Theo thông cáo kết quả dữ liệu nghiên cứu FDA thì cho thấy hiệu quả thực tế đối với người nhiễm COVID-19 có triệu chứng tại Mỹ đạt 76,7% sau 28 ngày tiêm. Vắc-xin đạt hiệu quả miễn dịch tại Nam Phi và Brazil là 64% đối với biến thể Beta và 68% đối với biến thể Gamma.
Vắc-xin này đã được Bộ Y tế phê duyệt sử dụng có điều kiện cho nhu cầu cấp bách trong phòng, chống dịch COVID-19. Hiện nay, Việt Nam chưa tiếp nhận vắc-xin này.
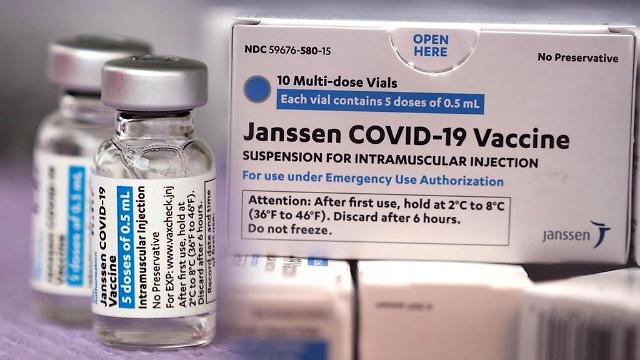
vắc-xin COVID-19 Janssen
Một số thông tin về vắc-xin phòng COVID-19 đầu tiên của Việt Nam- Nanocovax
Trong điều kiện cấp thiết cần có vắc-xin cho nhu cầu phòng chống đại dịch COVID-19, song song với các nỗ lực đàm phán mua vắc xin từ các nhà sản xuất nước ngoài, thực hiện chỉ đạo của Chính phủ về nghiên cứu, phát triển vắc xin phòng COVID-19 trong nước, Bộ Y tế đã tạo mọi điều kiện thuận lợi cho các nhà sản xuất vắc-xin trong nước, trong đó có Công ty Cổ phần công nghệ sinh học Dược Nanogen, đơn vị nghiên cứu, phát triển ứng viên vắc-xin Nanocovax.
Hiện nay, vắc-xin Nanocovax đang TNLS giai đoạn 2 của pha 3 và đã hoàn thành tiêm 2 mũi vắc xin cho 13.000 người tình nguyện của giai đoạn 3, dự kiến đến ngày 10/9/2021 sẽ hoàn thành các xét nghiệm đánh giá tính sinh miễn dịch sau 42 ngày tiêm vắc xin mũi 1 của giai đoạn 3a [2].
Nhìn chung, kết luận tại cuộc họp khẩn cấp hội đồng đạo đức trong nghiên cứu y sinh học quốc gia ngày 22/8/2021 xem xét kết quả giữa kỳ thử nghiệm lâm sàng giai đoạn 3a ứng viên vắc xin Nanocovaxcho thấy vắc-xin Nanocovax đạt yêu cầu về tính an toàn (ngắn hạn) dựa trên dữ liệu báo cáo kết quả giữa kỳ TNLS giai đoạn 3a tính đến thời điểm hiện tại và có tính sinh miễn dịch trên các xét nghiệm đã có kết quả, tuy nhiên, cần tiếp tục bổ sung kết quả xét nghiệm trung hòa vi rút SARS-CoV-2 sống trên nuôi cấy tế bào (PRNT) trên chủng Delta (phát hiện lần đầu tại Ấn Độ) và trên chủng Alpha (phát hiện lần đầu tại Anh) để đủ các kết quả xét nghiệm theo đề cương đã được phê duyệt. Mặc khác, chưa có dữ liệu để đánh giá trực tiếp hiệu lực bảo vệ của ứng viên vắc xin Nanocovax, cần tiếp tục thực hiên theo đề cương, đánh giá về hiệu lực bảo vệ theo đề cương được phê duyệt - đây là kết quả quan trọng nhất về chất lượng [2].
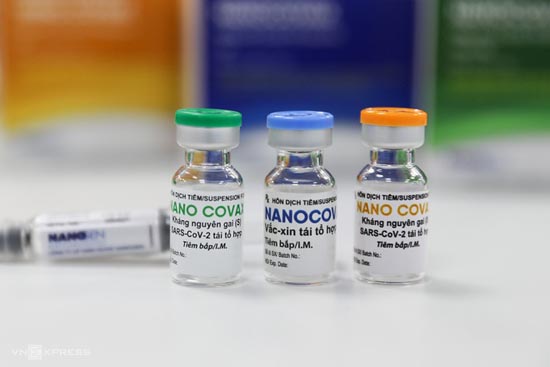
vắc-xin phòng COVID-19-Nanocovax.
Việc cấp phép sẽ dựa trên ý kiến tư vấn của Hội đồng đạo đức trong nghiên cứu y sinh học cấp quốc gia và ý kiến tư vấn của Hội đồng tư vấn cấp giấy đăng ký lưu hành thuốc, nguyên liệu làm thuốc, có tham khảo hướng dẫn hoặc khuyến cáo của Tổ chức Y tế thế giới.Trong thời hạn tối đa 20 ngày làm việc kể từ ngày nhận đủ hồ sơ đối với hồ sơ đề nghị cấp giấy đăng ký lưu hành vắc xin, Cục trưởng Cục Quản lý Dược sẽ cấp giấy đăng ký lưu hành vắc xin.Sau khi được cấp phép lưu hành, cơ sở đăng ký phải tiếp tục phối hợp với cơ sở sản xuất thực hiện nghiên cứu lâm sàng và cập nhật dữ liệu lâm sàng theo hướng dẫn của Bộ Y tế.
Như v
ậy, hiện nay, theo Tổ chức Y tế Thế giới, tiêm vắc-xin được đánh giá là biện pháp lâu dài để phòng chống dịch COVID-19. Vắc-xin không chỉ giúp bảo vệ cơ thể trước dịch bệnh COVID-19 mà còn giảm nguy cơ bệnh nặng hoặc tử vong khi mắc bệnh.Theo đó, việc đẩy nhanh việc người dân được tiêm vắc xin đầy đủ là giải pháp nhanh chóng nhất để đạt miễn dịch cộng đồng. Tất nhiên không có vắc-xin COVID-19 loại nào hiệu quả đạt tuyệt đối 100%, nhưng chúng có thể bảo vệ chúng ta và phần nào là lá chắn bảo vệ những người dễ bị tổn thương nhất bởi virus SARS-CoV-2. WHO lưu ý vẫn phải duy trì và tăng cường các biện pháp y tế công cộng hiệu quả: đeo khẩu trang, giãn cách, rửa tay, vệ sinh hô hấp và quy tắc che miệng khi ho, tránh tụ tập đông người, và đảm bảo thông khí tốt.
Thực hiện tốt thông điệp 5K và tiêm vắc-xin phòng COVID-19 là quyền lợi đối với bản thân
và là trách nhiệm đối với cộng đồngđể cùng nhau đẩy lùi dịch bệnh.
Vì vậy, dù đã được tiêm vắc-xin, cùng chung tay với Bộ Y Tế thực hiện 5K, bảo vệ bản thân và gia đình, nâng cao ý thứcphòng chống dịch đẩy lùi đại dịch - nhanh chóng phục hồi và phát triển kinh tế.
Tài liệu tham khảo:
1.Bộ Y tế, 6 loại vaccine phòng COVID-19 đã được cấp phép tại Việt Nam, https://moh.gov.vn/tin-lien-quan/-/asset_publisher/vjYyM7O9aWnX/content/6-loai-vaccine-phong-covid-19-a-uoc-cap-phep-tai-viet-nam.
2.Bô Y tế, Hội đồng Đạo đức nghiên cứu y sinh học Quốc gia: Vaccine Nanocovax đạt yêu cầu về tính an toàn, https://moh.gov.vn/tin-tong-hop/-/asset_publisher/k206Q9qkZOqn/content/hoi-ong-ao-uc-nghien-cuu-y-sinh-hoc-quoc-gia-vaccine-nanocovax-at-yeu-cau-ve-tinh-an-toan
3.https://www.who.int/vietnam/vi/news/detail/19-04-2021-the-oxford-astrazeneca-covid-19-vaccine-what-you-need-to-know
4.https://vnvc.vn/astrazeneca/
5.https://vnvc.vn/sputnik-v/
6.https://www.who.int/vietnam/vi/news/feature-stories/detail/the-sinopharm-covid-19-vaccine-what-you-need-to-know
7.https://www.who.int/vietnam/news/detail/06-07-2021-the-pfizer-biontech-(bnt162b2)-covid-19-vaccine-what-you-need-to-know
8.https://www.fda.gov/consumers/consumer-updates/5-dieu-ban-can-biet-ve-thuoc-chung-ngua-covid-19-cho-thanh-thieu-nien-tu-12-den-17-tuoi
9.https://www.cdc.gov/mmwr/volumes/69/wr/mm695152e1.htm?s_cid=mm695152e1_w (The Advisory Committee on Immunization Practices’ Interim Recommendation for Use of Moderna COVID-19 Vaccine — United States, December 2020)
10.https://vietnamese.cdc.gov/coronavirus/2019-ncov/vaccines/different-vaccines/janssen.html