Những con số này không bao gồm các trường hợp nhiễm sốt rét không triệu chứng, vốn cũng có thể ảnh hưởng đáng kể đến sức khỏe của người nhiễm bệnh (Chen và cs., 2016 ). Dự kiến số ca nhiễm sẽ chỉ tăng lên cùng với sự nóng lên toàn cầu (Caminade và cs., 2014 ). Bệnh sốt rét do ký sinh trùng Plasmodium spp. gây ra, ký sinh trùng này tăng sinh sôi và lây truyền qua muỗi Anopheles spp. cái, là vật chủ trung gian truyền bệnh. Trong số năm loài Plasmodium spp. gây bệnh sốt rét ở người, thì Plasmodium falciparum gây ra tỷ lệ tử vong cao nhất, trong khi P. vivax gây ra nhiều trường hợp mắc bệnh sốt rét nhất trong và ngoài châu Phi. Có khoảng 515 loài muỗi Anopheles spp., trong đó khoảng 30 đến 40 loài được coi là vật chủ trung gian truyền bệnh sốt rét quan trọng (WHO, 2020).
Cho đến thế kỷ 20, bệnh sốt rét phổ biến ở hơn một nửa thế giới. Từ đó trở đi, con người mới đạt được tiến bộ trong việc chống lại căn bệnh này. Sốt rét là bệnh đặc hữu ở châu Âu cho đến những năm 1970, với Macedonia là quốc gia cuối cùng loại trừ được bệnh này vào năm 1975 (Piperaki và cs., 2018 ). Đến năm 2002, bệnh sốt rét chỉ còn hiện diện ở 27% diện tích đất liền toàn cầu (Hay và cs., 2004 ). Điều này cho thấy sốt rét không phải là bệnh đặc hữu của vùng nhiệt đới mà là một căn bệnh đã được loại trừ ở khắp mọi nơi ngoại trừ vùng nhiệt đới. Ngày nay, sốt rét là bệnh đặc hữu ở 87 quốc gia, với khu vực châu Phi của TCYTTG chiếm 94% số ca mắc và tử vong do sốt rét trên toàn cầu (WHO, 2020).Kiểm soát vật chủ trung gian truyền bệnh là một phần thiết yếu trong các biện pháp can thiệp y tế công cộng (YTCC) chống lại bệnh sốt rét, vì việc loại bỏ ký sinh trùng Plasmodium spp. một cách riêng lẻ đã được chứng minh là rất khó khăn. Ký sinh trùng Plasmodium spp. gây bệnh sốt rét là những sinh vật rất phức tạp với nhiều giai đoạn sống và sinh sản khác nhau cả trong cơ thể muỗi và ở cơ thể người.
Rất nhiều nỗ lực đã được đầu tư vào việc phát triển vaccine nhắm vào ký sinh trùng (KST) này, với vaccine RTS,S gần đây là loại chống sốt rét đầu tiên được đưa ra thị trường, nhưng một loại vaccine có hiệu quả cao và cung cấp khả năng bảo vệ trong thời gian dài khó có thể sớm có mặt (Feachem và cs., 2019; WHO, 2021 ). Do đó, sự suy giảm bệnh sốt rét đạt được cho đến nay là nhờ những nỗ lực lớn về YTCC tập trung vào phòng ngừa thông qua việc sử dụng hóa chất, giảm các địa điểm sinh sản của muỗi và phát triển kinh tế xã hội (Roser và Ritchie, 2019 ). Tuy nhiên, tỷ lệ mắc bệnh sốt rét vẫn chưa giảm đáng kể trong những năm gần đây, một trong những lý do là sự phát triển của muỗi kháng hóa chất (WHO, 2020). Đã có những tiến bộ, nhưng việc xóa sổ hoàn toàn vẫn còn xa vời, nên các nhà nghiên cứu đang theo đuổi những khả năng khác.
Phân tích hệ gen của muỗi Anopheles spp. có giá trị cốt lõi trong loại trừ sốt rét (LTSR) bằng cách xác định các gen kháng hóa chất, hiểu rõ hành vi sinh học và sinh thái của muỗi sốt rét và phát triển các công nghệ di truyền mới như chỉnh sửa gen CRISPR (Clustered Regularly Interspaced Short Palindromic Repeats)để giảm khả năng lây truyền hoặc tiêu diệt quần thể muỗi mang bệnh. Giá trị cụ thể của phân tích genomic muỗi Anopheles spp.Nhìn chung, phân tích hệ gen giúp chuyển đổi từ các phương pháp kiểm soát muỗi đại trà sang các chiến lược chính xác, bền vững và hiệu quả cao hơn trong nỗ lực LTSR.
- Phát triển công nghệ di truyền (Gene Drive/CRISPR): Phân tích hệ gen cho phép xác định và chỉnh sửa các gen liên quan đến khả năng miễn dịch hoặc sự phát triển của muỗi, giúp tạo ra các dòng muỗi kháng ký sinh trùng Plasmodium spp. hoặc giảm khả năng sinh sản của chúng. Ví dụ, phát hiện biến thể gen FREP1 giúp tạo ra muỗi kháng ký sinh trùng P. falciparum;
- Hiểu về cơ chế kháng hóa chất diệt côn trùng: Phân tích hệ gen giúp xác định các gen chịu trách nhiệm cho khả năng kháng hóa chất, từ đó giúp xây dựng các chiến lược quản lý kháng hóa chất hiệu quả hơn;
- Phân biệt các loài muỗi và biến thể: Giúp nhận diện chính xác các loài Anophelesspp. truyền bệnh chính (như An. gambiae, An. dirusở châu Phi và châu Á) và các biến thể phân tử (dạng M và S) để tập trung nguồn lực kiểm soát đúng đối tượng;
- Nghiên cứu hành vi và sinh thái: Hiểu rõ hành vi hút máu (ưa đốt máu người hay máu gia súc), thời gian hoạt động và môi trường sống của muỗi để tối ưu hóa các biện pháp can thiệp truyền thống;
- Dự đoán mô hình dịch tễ học: Sử dụng dữ liệu di truyền để đánh giá khả năng truyền bệnh của quần thể muỗi, thay thế một phần cho các cuộc khảo sát huyết thanh học trên người.
Năm 2014, một công nghệ mới được giới thiệu kết hợp giữa cơ chế điều khiển gen (gene drive) và hệ thống CRISPR-Cas9. Cơ chế điều khiển gen là một phương pháp biến đổi gen cho phép một số gen nhất định lan truyền trong quần thể bằng cách tăng tỷ lệ di truyền của chúng. Thông thường, một biến đổi gen dị hợp tử được di truyền ở 50% con cái. Tuy nhiên, khi kết hợp với CRISPR-Cas9, biến đổi gen này cũng được sao chép sang nhiễm sắc thể tương đồng, dẫn đến sự hiện diện đồng hợp tử của biến đổi này. Điều này có nghĩa là đột biến sẽ có mặt trong cả hai bản sao của cặp nhiễm sắc thể. Bằng cách này, đột biến được di truyền ở 100% con cái, trong đó nó lại được sao chép sang nhiễm sắc thể tương đồng và các gen bị biến đổi lan truyền nhanh hơn nữa (Esvelt và cs., 2014; Hayirli và Martelli, 2019; Scudellari và cs., 2019 ). Năm 2018, Kyrou và cộng sự đã phát triển một cơ chế điều khiển gen dựa trên CRISPR liên quan đến gen doublesex.
Kỹ thuật này tập trung vào muỗi An. gambiae, một loài muỗi truyền bệnh ký sinh trùng P. falciparum. Khi gen này bị vô hiệu hóa ở muỗi cái, chúng phát triển cả cơ quan sinh dục đực và cái. Vòi hút của chúng chuyển thành vòi hút của con đực, khiến chúng không thể chích hút da người và trở nên vô sinh. Kỹ thuật này tập trung vào muỗi Anopheles cái vì ngoài mật hoa (tất cả các loài Anopheles đều ăn), chúng còn cần máu để lấy protein cho quá trình đẻ trứng. Muỗi Anopheles spp. đực không thể chích hút da và truyền bệnh do Plasmodium spp. Khi gen lưỡng tính được đưa vào quần thể muỗi Anopheles spp. nuôi nhốt, quần thể này đã chết sau bảy đến mười một thế hệ (Kyrou và cs., 2018). Nếu những con muỗi biến đổi gen này được đưa vào tự nhiên, điều này có thể dẫn đến sự tuyệt chủng của toàn bộ loài mục tiêu. Do đó, kỹ thuật này có cơ hội tốt để góp phần xóa sổ bệnh sốt rét, vì ký sinh trùng khó tìm được vật chủ trung gian mới (Callaway và cs., 2015; Hammond và cs., 2017).
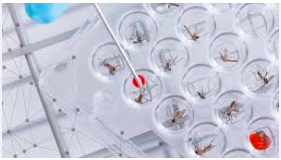
Hình 2. Muỗi biến đổi gen – Tốt hay không tốt
|Nguồn: https://www.mosquitomagnet.com/articles/gmo-mosquitoes-pros-cons?
Do những tác động bất lợi mà công nghệ này có thể gây ra cho môi trường, việc sử dụng công nghệ dẫn truyền gen đã vấp phải nhiều chỉ trích (Brossard và cs., 2019). Tác động trực tiếp thông qua việc xóa sổ một loài hoặc tác động gián tiếp thông qua lai giống có thể dẫn đến những hậu quả khó lường đối với sức khỏe con người và môi trường. Các khả năng bao gồm thay đổi động lực hệ sinh thái hoặc sự lan truyền gen sang các loài khác (Neves và Druml, 2017). Đến nay, kỹ thuật này chỉ được sử dụng trong môi trường được kiểm soát, nhưng muỗi biến đổi gen có thể sớm được thả vào tự nhiên. Quỹ Bill và Melinda Gates đã đầu tư vào việc tìm kiếm giải pháp dẫn truyền gen và Bill Gates hy vọng sẽ nhận được sự chấp thuận của cơ quan quản lý vào năm 2024 và có những con muỗi dẫn truyền gen đầu tiên sẵn sàng vào năm 2026 (Gates và cs., 2019 ). Trước khi điều này xảy ra, các vấn đề đạo đức cần được xem xét kỹ lưỡng.Bài viết này sẽ thảo luận về các mối quan ngại đạo đức khác nhau phát sinh liên quan đến việc diệt trừ một loài muỗi sốt rét thông qua kỹ thuật di truyền dựa trên cơ chế điều khiển gen. Cuộc thảo luận sẽ liên quan đến:
(a) Giá trị của một loài;
(b) Tác động môi trường do cả việc diệt trừ muỗi A. gambiae và việc sử dụng cơ chế điều khiển gen;
(c) Tầm quan trọng của sự tham gia của cộng đồng. Điều này sẽ làm sáng tỏ những phức tạp và góp phần đưa ra quyết định sáng suốt về việc thực hiện biện pháp này.
Đa dạng sinh học theo truyền thống được định nghĩa là “Sự đa dạng của sự sống, trong tất cả biểu hiện khác nhau của nó” (Sodhi và Ehrlich, 2010). Nó có nhiều giai đoạn và bao gồm sự đa dạng của gen, loài, quần thể và toàn bộ hệ sinh thái (Carrington và cs., 2019 ). Như đã mô tả ở trên, kỹ thuật được đề xuất có thể dẫn đến việc “tuyệt chủng” một loài và do đó làm giảm đa dạng sinh học. Tuy nhiên, bảo tồn đa dạng sinh học là mục tiêu của nhiều tổ chức và chính phủ (Quỹ Bảo tồn Động vật hoang dã Thế giới (WWF) 2015; Ủy ban Châu Âu 2017; IUCN, 2020; Liên hợp Quốc, 2020 ). Đa dạng sinh học rất cần thiết cho nhiều lợi ích cho thế giới, bao gồm cung cấp thực phẩm, lọc nước, ổn định khí hậu trái đất và lợi thế thẩm mỹ, cùng nhiều lợi ích khác (WWF, 2015 ). Đa dạng sinh học được coi là có giá trị lớn đối với thế giới, nhưng điều này có nghĩa là tất cả loài đều có giá trị và nên được bảo vệ?
Rõ ràng là không phải tất cả sinh vật đều được đối xử bình đẳng. Sinh vật bao gồm mọi dạng sống, trong khi động vật là các sinh vật đa bào cụ thể, không phải thực vật hoặc nấm. Các sinh vật đơn bào thường không được đưa vào các chương trình bảo vệ sự sống, dù chúng có tỷ lệ tuyệt chủng cao (Weinbauer và Rassoulzadegan, 2007; Louca và cs., 2018 ). Việc loại trừ virus, vốn nằm trong vùng xám giữa sự sống và không sống, từ lâu đã được coi là một thắng lợi: virus đậu mùa đã được loại trừ từ năm 1980, nhờ những nỗ lực lớn của YTCC. Điều này đã mang lại lợi ích to lớn cho nhân loại và một cách chính đáng đã được ca ngợi (CDC, 2016 ). Việc loại trừ virus SARS-CoV-2 gần đây chắc chắn cũng sẽ được ca ngợi trên toàn cầu. Giun rồng đã là trọng tâm của chương trình xóa sổ toàn cầu từ năm 1980. Với chỉ 28 trường hợp được báo cáo vào năm 2018, giun rồng có khả năng trở thành loài bị xóa sổ có chủ đích thứ hai vì mục đích sức khỏe cộng đồng (CDC, 2019).
Tuy nhiên, việc loại bỏ KSTSR vẫn chưa phải là một lựa chọn. Thay vào đó, việc phòng ngừa sốt rét thông qua việc nhắm mục tiêu vào muỗi đã trở thành trọng tâm chính. Tuy nhiên, tầm quan trọng của việc bảo tồn côn trùng và cụ thể hơn là muỗi, vẫn chưa được xác định rõ ràng. Trong thế giới động vật, cái gọi là “các loài bậc cao”- động vật có xương sống khác ngoài cá - đã là trọng tâm của các chương trình bảo tồn (CITES, 2011; World Animal Protection, 2018; Pandas International, 2020; Save the Rhino, 2020). Câu hỏi đặt ra là ranh giới giữa việc tuyệt chủng một loài có thể chấp nhận được về mặt đạo đức và không thể chấp nhận được nằm ở đâu.
Hình 3. Brazil thả hàng tỷ con muỗi phát triển từ phòng Lab theo dự án muỗi biến đổi gen của Oxitec tại Piracicaba, Brazil
|Nguồn: Paulo Freidman, 2021
Theo trực giác, ý tưởng cho rằng tất cả sinh vật hoặc động vật đều bình đẳng, bất kể loài của chúng, không phải là nhận thức phổ biến của phần lớn dân số thế giới. Phản ứng của công chúng đối với việc tiêu diệt một loài phụ thuộc chủ yếu vào vị thế đạo đức của sinh vật đó cũng như những hậu quả có thể xảy ra khi việc tiêu diệt nó diễn ra (Pugh và cs., 2016). Khi một nghiên cứu ở Thụy Điển hỏi người dân về việc sử dụng hóa chất chống muỗi, nhiều người trả lời rằng họ không muốn loại bỏ toàn bộ loài này vì điều đó sẽ cảm thấy sai trái về mặt đạo đức (Ojala và Lidskog, 2011 ). Tuy nhiên, trong trường hợp này, loài muỗi này chỉ gây ra những phiền toái nhỏ chứ không phải hàng trăm nghìn cái chết.
Muỗi, với tư cách là một loài, thường được gán cho địa vị đạo đức thấp hoặc thậm chí là không có địa vị đạo đức nào (tên gọi Anopheles spp., có nghĩa là vô dụng trong tiếng Hy Lạp, càng làm trầm trọng thêm vấn đề này). Cũng có sự khác biệt giữa việc giết một vài con muỗi và việc cố ý tiêu diệt toàn bộ một loài muỗi. Địa vị đạo đức không phải là vấn đề trắng đen mà là vấn đề về mức độ (DeGrazia và cs., 2008). David DeGrazia phân biệt mô hình hai cấp độ với mô hình thang trượt, như những cách giải thích về việc gán địa vị đạo đức. Trong mô hình hai cấp độ này, con người được gán địa vị đạo đức trong khi các sinh vật có tri giác khác có địa vị đạo đức thấp hơn nhưng không bao giờ hoàn toàn không có địa vị đạo đức. Sử dụng mô hình thang trượt, mức độ địa vị đạo đức mà một sinh vật được dành cho phụ thuộc vào mức độ phức tạp về nhận thức, cảm xúc và xã hội của chúng. Theo mô hình này, con người được gán địa vị đạo đức cao nhất và các sinh vật không có tri giác được gán địa vị thấp nhất. Tương tự, Peter Singer phân loại các sinh vật thành các nhóm khác nhau tùy thuộc vào khả năng cảm nhận và tự nhận thức. Các sinh vật có tri giác và tự nhận thức xứng đáng được xem xét đầy đủ về mặt đạo đức trong khi các sinh vật không có tri giác thì không (BBC, 2014).
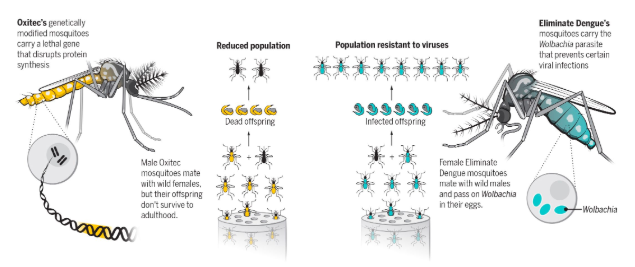
Hình 4. Muỗi nuôi trong phòng Lab được thử nghiệm tại Brazil bởi dự án Oxitec and Eliminate Dengue nhằm ngăn chặn tác nhân gây bệnh
|Nguồn: https://www.science.org/content/article/brazil-will-release-billions-lab-grown-mosquitoes-combat-infectious-disease-will-it
Những người tin rằng tất cả loài đều có giá trị nội tại lại có quan điểm khác. Theo nhà sinh vật học Michael Soulé “Các loài có giá trị tự thân, một giá trị không được ban tặng cũng không thể thu hồi, mà bắt nguồn từ di sản tiến hóa lâu dài và tiềm năng của loài đó”. Ý tưởng này được nhiều nhà bảo tồn khác ủng hộ và tương đương với triết lý của Tom Regan rằng tất cả loài đều có giá trị nội tại vì chúng là chủ thể của sự sống (Regan và cs., 2004). Tuy nhiên, Regan chỉ nói về động vật, chứ không phải sinh vật. Không rõ liệu côn trùng cũng có thể được coi là chủ thể của sự sống hay không vì chưa rõ chúng có ý thức ở mức độ nào, hoặc thậm chí có thể cảm nhận được đau đớn hay không. Ngay cả khi một số côn trùng có phần nào đó có tri giác và bằng chứng chỉ ra theo hướng ngược lại, liệu điều đó có nghĩa là chúng nên được bảo vệ? Bản thân Singer cho rằng, bất kể tri giác của chúng, một chiến dịch bảo vệ quyền của côn trùng vẫn chưa nằm trong chương trình nghị sự (Singer, 2016 ). Như vậy, dựa trên quan điểm của Singer và Regan, việc đấu tranh cho quyền của muỗi là không cần thiết.
Về thước đo định lượng của đa dạng sinh học, cần lưu ý bệnh sốt rét chỉ do khoảng 30-40 loài muỗi Anopheles spp. gây ra. Vì có hơn 3500 loài muỗi, việc tiêu diệt 30 loài Anopheles spp. đó chỉ làm giảm đa dạng sinh học của tất cả loài muỗi đi một phần trăm (AMCA, 2019 ). Hơn nữa, loài muỗi mà gen lưỡng tính bị vô hiệu hóa vào năm 2018 là muỗi A. gambiae. Việc tiêu diệt riêng loài này hầu như không ảnh hưởng đến tổng đa dạng sinh học của muỗi.Một vấn đề đáng lo ngại khác là nếu một số loài được bảo vệ và một số loài bị tiêu diệt có chủ đích, điều này có thể dẫn đến các chương trình tiêu diệt nhiều loài khác nhau: Một tiền lệ nguy hiểm. Thật vậy, việc tiêu diệt một loài muỗi có thể tạo tiền lệ để biện minh cho việc tiêu diệt các loài muỗi khác. Tập trung vào việc tiêu diệt các loài muỗi truyền bệnh sốt xuất huyết, sốt vàng da hoặc Zika là bước tiếp theo hợp lý nếu việc tiêu diệt muỗi A. gambiae thành công.
Xét đến thang bậc đạo đức và quan điểm về muỗi như những sinh vật không có tri giác, đã được thảo luận ở các đoạn trước, dường như việc hy sinh muỗi để cứu mạng sống con người là được phép về mặt đạo đức. Tuy nhiên, chức năng của một loài luôn phải được tính đến và các khả năng khác để loại trừ những căn bệnh này cũng phải được xem xét. Việc tiêu diệt một loài chỉ được phép nếu nó cứu được một số lượng đáng kể mạng sống con người hoặc bảo vệ hệ sinh thái, nếu không còn cách nào khác. Việc tiêu diệt không bao giờ nên là lựa chọn đầu tiên mà phải là lựa chọn cuối cùng.
(còn nữa) --> Tiếp theo Phần 2
TS.BS. Huỳnh Hồng Quang& CN. Nguyễn Thái Hoàng
Viện Sốt rét-KST-CT Quy Nhơn