|
Leishmania donovani: Loài ký sinh trùng đơn bào gây bệnh truyền nhiễm ở người đang nổi tại Việt Nam? (Phần 2)
Phần 1: Leishmania donovani: Loài ký sinh trùng đơn bào gây bệnh truyền nhiễm ở người đang nổi tại Việt Nam?
CHU KỲ SINH HỌC VÀ PHÁT TRIỂN Chu kỳ phát triển của Leishmania spp. phải qua hai vật chủ: Vật chủ vĩnh viễn là người (động vật), vật chủ trung gian là là muỗi cát Phlebotomus.Khi muỗi cát đốt người (động vật) bệnh hút máu, hút luôn thể amastigote (dạng không roi) vào dạ dày của nó. Trong ruột muỗi cát, ký sinh trùng đơn bào sẽ chuyển từ dạng không roi sang dạng có roi (promastigote), tăng sinh và sau đó sẽ di chuyển lên vòi muỗi cát, không xâm nhập vào tuyến nước bọt. Trong vòng 8 - 15 ngày, thể này có khả năng gây nhiễm. Khi muỗi cát đốt người (động vật) sẽ truyền ký sinh trùng này vào vật chủ. Giai đoạn ở động vật có xương sống Vật chủ là người, chó, mèo, cáo và những động vật ăn thịt khác. Leishmania spp. ký sinh ở trong tế bào thuộc hệ thống võng mạc nội mô của các phủ tạng như gan, lách, hạch, tủy xươngvà trong bạch cầu đơn nhân. Trong tế bào, Leishmania spp. sinh sản vô giới, khi đạt đến số lượng lớn, Leishmania spp. phá vỡ tế bào mà chúng đang ký sinh, rồi lại xâm nhập vào các tế bào khác. Cứ như thế, ký sinh trùng đơn bào Leishmania spp. phát triển, đồng thời gây tổn thương các nội tạng vật chủ. Leishmania spp. lấy các chất dinh dưỡng từ mô vật chủ, chủ yếu là dextrose rất cần cho sự phát triển của Leishmania. Mọi chuyển hoá của Leishmania theo đường ái khí, sử dụng O2 từ dextrose. Giai đoạn ở động vật không xương sống: Muỗi cát đốt người và động vật hút máu có cả Leishmania spp. vào dạ dày muỗi. Ở dạ dày muỗi cát, từ thể không roi Leishmania spp. biến thành thể có roi Leptomonas, rồi xâm nhập vào các tế bào dạ dày muỗi cát. Ở đây, Leishmania spp. sinh sản vô giới, đạt tới mức số lượng lớn, phá hủy tế bào dạ dày, di chuyển tới họng và vòi muỗi. Khi muỗi cát đốt người và động vật, chúng sẽ truyền các thể có roi vào người và động vật. Tại vật chủ mới, các thể có roi sẽ chuyển thành thể không roi ký sinh và gây bệnh.
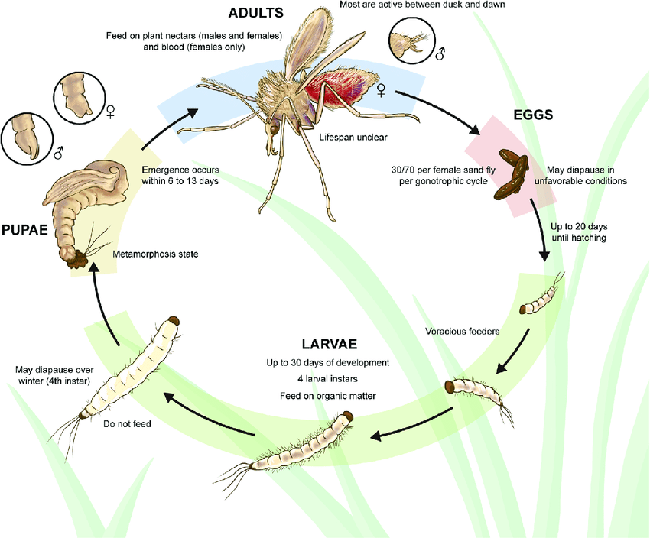
Hình 4. Chu kỳ sinh học và phát triển của muỗi cát bao gồm 4 giai đoạn chính: Trứng (màu cam), ấu trùng (4 lần lột xác instars: màu xanh lá cây), nhộng (màu vàng) và trưởng thành (m
àu xanh da trời).
Trong hai giai đoạn sau, các đặc điểm về hình thái khác nhau (đặc trưng trong cái vòng tròn)có thể dùng để phân biệt giới tính.
Đặc điểm quan trọng nhất ở mỗi giai đoạn được mô tả gần hình ảnh cũng như thời gian trung bình phát triển giai đoạn đó.
Nguồn: NIAID, 2022.
BỆNH HỌC Có nhiều hình thức khác nhau của bệnh do Leishmaniaspp. ở người. Ở một số người, bệnh diễn tiến âm thầm, không có bất kỳ triệu chứng hoặc dấu hiệu nào. Tùy theo nơi định vị của ký sinh trùng đơn bào Leishmania spp., người ta phân biệt được các thể lâm sàng như sau: - Thể ở da:Là thể phổ biến nhất của bệnh, ký sinh trùng gây lở loét da. Các vết loét thường phát triển trong một vài tuần hay vài tháng sau khi muỗi cát đốt. Vết loét có thể thay đổi kích thước và hình dạng theo thời gian, có thể bắt đầu ra như là sẩn hoặc nốt (cục u) và có thể kết thúc như loét (giống như một ngọn núi lửa, với một cạnh nâng lên và miệng núi lửa trung tâm); loét da có thể được bao phủ bởi một lớp vảy. Các vết loét thường là không đau nhưng một số trường hợp có thể đau. Một số có sưng hạch ở gần vết loét (dưới cánh tay, nếu vết loét trên cánh tay hoặc bàn tay). Bệnh do Leishmania da còn được gọi là “Đau vùng nhiệt đới”, “Nhọt phương Đông”, Delhi hoặc Aleppo, Uta hoặc loét Chiclero, hoặc bệnh ghẻ rừng. Các loài gây bệnh chính gồm L. major và L. tropica ở Nam Âu, Châu Á và Châu Phi; loài L. mexicana và các loài liên quan ở Mexico và Trung và Nam Mỹ; loài L. braziliensis và các loài liên quan ở Trung và Nam Mỹ. Các ca bệnh đã xảy ra giữa các nhân viên quân sự Mỹ phục vụ ở Iraq và Afghanistan và trong số những người đi du lịch đến các vùng lưu hành ở Trung và Nam Mỹ, Israel và các nơi khác. Không phổ biến, L. braziliensis lan rộng trong da gây bệnh do Leishmaniaspp. lan tỏa trên da. Trong bệnh do Leishmania spp. da, tổn thương da được phân định rõ tiến triển ở vùng bị ruồi cát đốt, thường là trong vài tuần tới vài tháng. Nhiều tổn thương có thể xảy ra sau nhiều vết đốt nhiễm trùng hoặc với sự lan truyền lan rộng. Hình thái của chúng khác nhau, tổn thương ban đầu thường là một đốm nở từ từ, loét ở giữa và phát triển một đường nướu tăng, hồng ban nơi ký sinh trùng nội bào tập trung. Vết loét thường không đau và không gây triệu chứng toàn thân trừ khi bị nhiễm lần thứ hai. Vết thương tự lành sau vài tháng nhưng có thể tồn tại trong nhiều năm, để lại một vết sẹo như cháy. Diễn biến bệnh phụ thuộc vào loài Leishmania spp. và trạng thái miễn dịch của cơ thể. 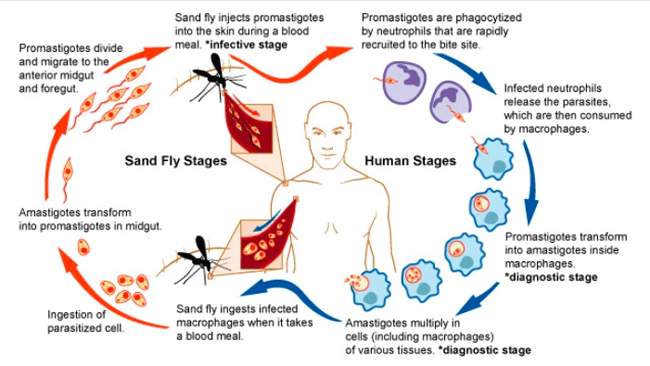
Hình 5. Con đường dẫn đến bệnh sinh của bệnh do Leishmania spp. ở người
- Thể ở da-niêm mạc: Hình thức này ít phổ biến, là một di chứng của bệnh do Leishmania spp. một số loại ký sinh trùng có thể lây lan từ da và gây ra lở loét ở niêm mạc mũi (phổ biến nhất), miệng hoặc cổ họng. Cách tốt nhất để ngăn chặn thể da-niêm mạc là phải điều trị hiệu quả nhiễm trùng da ban đầu.Bệnh chủ yếu là do L. braziliensis nhưng đôi khi bởi các loài Leishmania khác. Các ký sinh trùng được cho là lây lan từ tổn thương da ban đầu thông qua các hạch bạch huyết và máu đến các mô vòm họng. Triệu chứng và dấu hiệu của bệnh do Leishmaniaspp. niêm mạc thường xuất hiện hàng tháng đến nhiều năm sau khi có sự xuất hiện tổn thương da.Bệnh do Leishmaniaspp. niêm mạc do L. braziliensis và các sinh vật liên quan thường bắt đầu bằng một hoặc nhiều vết loét nguyên phát trên da. Lây lan đến niêm mạc qua đường bạch huyết và đường máu có thể xuất hiện sớm trong thời kỳ nhiễm bệnh. Tổn thương da này lành một cách tự nhiên; nhưng tổn thương niêm mạc tiến triển có thể không trở nên rõ ràng trong nhiều năm. Thông thường, bệnh nhân có nghẹt mũi, chảy máu và đau. Theo thời gian, nhiễm trùng có thể tiến triển, dẫn đến loét hoàn toàn mũi, vòm miệng, miệng họng hoặc mặt. 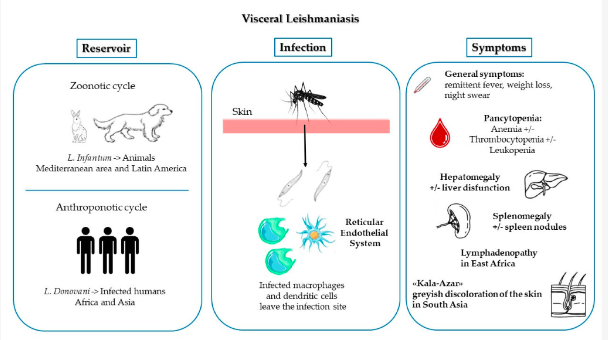
Hình 6. Chu kỳ sinh học do L. infantum vàL. donovani và triệu chứng bệnh chính thể nội tạng ở người
- Thể ở nội tạng: Bệnh ảnh hưởng nhiều cơ quan nội tạng (lách, gan và tủy xương) và có thể đe dọa tính mạng. Bệnh thường phát triển trong vòng nhiều tháng (đôi khi nhiều năm) sau khi muỗi cát đốt. Đặc trưng bởi những cơn sốt bất thường, sụt cân, gan to, lách to và thiếu máu.Bệnh do Leishmania lan tỏa, một hội chứng hiếm gặp, kết quả là tổn thương da nốt lan rộng lan rộng giống như bệnh Phong. Nó phát sinh từ sự dị ứng qua trung gian tế bào với cơ thể. L.donovani gây bệnh phủ tạng và chia làm 3 thể và có 3 dưới loài của L. donovani gây ra: + Bệnh Kala-Azar còn gọi là thể Ấn Độ, hay gọi là bệnh sốt đen, do L.donovanigây ra; + Bệnh Kala-Azar trẻ em, còn gọi là thể Địa Trung Hải, do mầm bệnh do L.donovani infantum; + Bệnh do Leishmania phủ tạng Đông Phi, còn gọi là thể châu Phi, do mầm bệnh do L.donovani archibadigây ra. Bệnh thể Leishmania nội tạng (Kala-Azar, hay sốt Dumdum) thường do L. donovani hoặc là L. infantum (trước đây gọi là L. chagasi ở Mỹ Latinh) và xảy ra ở Ấn Độ, châu Phi (đặc biệt là Sudan), Trung Á, lưu vực Địa Trung Hải, Nam và Trung Mỹ và ít gặp ở Trung Quốc. Hầu hết các ca xảy ra ở vùng đông bắc Ấn Độ. Ký sinh trùng lan rộng từ vết đốt vào da đến các hạch vùng bạch huyết, lách, gan và tủy xương và gây ra các triệu chứng toàn thân. Biểu hiện nhiễm trùng thường gặp trên xét nghiệm cận lâm sàng; chỉ có một số ít bệnh nhân mắc bệnh tiến triển thành bệnh do Leishmania spp. nội tạng. Triệu chứng nhiễm trùng với L. infantum là phổ biến hơn ở trẻ em so với người trưởng thành. Bệnh do Leishmania nội tạng là một bệnh nhiễm trùng cơ hội ở bệnh nhân AIDS hoặc bệnh suy giảm miễn dịch khác. Trong thể nội tạng, biểu hiện lâm sàng thường phát triển dần dần trong vòng vài tuần đến vài tháng sau khi bi nhiễm ký sinh trùng nhưng có thể cấp tính. Sốt không thường xuyên, gan lách to, giảm hồng cầu, bạch cầu, tăng globulin miễn dịch đa dòng và đảo ngược tỷ lệAlbumin/Globulin miễn dịch. Ở một số bệnh nhân, sốt cao có đỉnh hai lần mỗi ngày. Tổn thương da hiếm khi xảy ra. Sự nhồi máu và tử vong xảy ra trong vòng vài tháng cho những bệnh nhân bị nhiễm trùng tiến triển. Những người có các bệnh nhiễm trùng không triệu chứng, tự khỏi và những người sống sót sau khi điều trị thành công có khả năng đề kháng với các đợt nhiễm khác trừ khi sự miễn dịch qua trung gian tế bào bị suy giảm. Tái phát có thể xảy ra hàng năm sau khi nhiễm trùng ban đầu. - Bệnh do Leishmania sau kala-azar (PKDL): Có thể xuất hiện sau khi điều trị bệnh do Leishmania spp. thể nội tạng ở Sudan và Ấn Độ. Nó được đặc trưng bởi tổn thương da phẳng hoặc nốt sần có chứa nhiều ký sinh trùng. Ở những bệnh nhân ở Sudan, những tổn thương này phát triển ở giai đoạn cuối hoặc trong vòng 6 tháng sau điều trị và tự nhiên khỏi sau vài tháng đến một năm. Ở các bệnh nhân ở Ấn Độ và các quốc gia lân cận, các tổn thương ở da thường phát triển từ 1 đến 2 năm sau khi kết thúc điều trị và có thể kéo dài trong nhiều năm. Tổn thương PKDL được coi là một nguồn lây nhiễm ở những khu vực này. PHÁT HIỆN & CHẨN ĐOÁN - Khám lâm sàng chuyên khoa hoặc hội chẩn chuyên khoa để khai thác đúng, đủ bệnh sử và tiền sử nghi ngờ nhiễm tác nhân gây bệnh. Đặc biệt, các vùng bệnh lưu hành bệnh do Leishmania spp. Leishmania spp. gây ra 3 thể và có 3 chủng, mỗi một chủng Leishmania sẽ gây ra một loại hình thái bệnh khác nhau trên lâm sang với các đối tượng độ tuổi khác nhau và địa phương khác nhau: L. donovani gây bệnh Kala-Azar:Nguồn bệnh là người, mọi lứa tuổi đều bị mắc bệnh, nhưng tỉ lệ bệnh cao hơn ở người lớn. Bệnh có biểu hiện các triệu chứng lâm sàng như sốt cao 39-400C, biểu đồ sốt làn sóng. Gan, lách sưng to nhanh trong phạm vi 3-6 tháng. Da bệnh nhân có màu sẫm, tóc giòn. Bạch cầu, hồng cầu giảm nhiều. Sau khi mắc bệnh, nếu bệnh nhân thoát tử vong, trên da xuất hiện những mụn gọi là “thể Leishmaniod”, trong mụn chứa nhiều Leishmania spp. L. donovani infantum gây bệnh Kala-Azar trẻ em: Bệnh thường gặp ở trẻ em, nguồn bệnh ngoài người ra còn chó, chuột, sóc, chồn, cáo…Bệnh biểu hiện sớm với các vết loét ở da, đường kính khoảng 2 cm, sau đó xuất hiện các triệu chứng như bệnh Kala-Azar ở người lớn như sốt cao, sốt làn sóng, gan lách sưng to, da sẫm màu… nhưng giai đoạn sau không xuất hiện Leishmaniod. L. donovani archibadi gây bệnh Leishmania spp. phủ tạng Đông Phi: Nguồn bệnh là người và động vật có vú hoang dại (động vật ăn thịt và động vật gậm nhấm). Bệnh xuất hiện những nốt mụn trên da, sau trở thành vết loét. Bệnh nhân sốt, gan, lách sưng to, da sẫm, có thể Leishmaniod ở da sau khi lui bệnh. - Xét nghiệm máu: Tốc độ lắng máu (VSS) thường tăng, từ 80-100mm giờ đầu. Tăng tỷ lệ globulin, đều này làm cho tỷ lệ albumin/globulin <1,0. Công thức máu toàn phần thấy thiếu máu đẳng sắc và bất sản, bạch cầu giảm chung, chủ yếu là bạch cầu đa nhân trung tính, giảm cả tiểu cầu trong nhiều ca bệnh trên lâm sàng; - Tìm ký sinh trùng đơn bào Leishmania spp.: + Thể da-niêm mạc: Lấy bệnh phẩm ở bìa sang thương (hoặc lấy dịch tiết, hoặc làm sinh thiết) làm phết mỏng và nhuộm bằng May - Grunwald - Giemsa; + Thể nội tạng: Chọc dò tủy xương ức hoặc chọc dò lách để tìm ký sinh trùngLeishmania spp. Trong trường hợp soi trực tiếp không tìm thấy ký sinh trùng thì nên cấy bệnh phẩm trong môi trường Novy-MacNeal-Nicolle(NNN) hai pha, soi bệnh phẩm thấy Leishmaniaspp. sẽ xuất hiện dưới dạng có roi (promastigote). Nhiễm trùng ở người có thể do 20 loài Leishmania spp. mà không thể phân biệt được hình thái học dễ dàng, nhưng có thể phân biệt bằng các phân tích trong phòng thí nghiệm. 
Hình 8.Các thể bệnh doLeishmania spp. và cơ quan bị ảnh hưởng;
Thể da niêm mạc phối hợp thể da, thể nội tạng ở gan và lách bị nhiễm và thể ở da bị nhiễm
Ngoài ra, còn có thể chẩn đoán gián tiếp bằng các phương pháp huyết thanh miễn dịch, nhất là phương pháp miễn dịch huỳnh quang, các thử nghiệm này cho kết quả dương tính trong 99% các trường hợp bị nhiễm.Các kỹ thuật dựa vào PCR (PCR-based techniques), vật dò hoặc tìm kháng thể đơn dòng tỏ ra có nhiều triển vọng trong chẩn đoán. Qua nghiên cứu gần đây, chẩn đoán bằng các phương pháp huyết thanh miễn dịch như phản ứng ngưng kết hạt trực tiếp, miễn dịch men, miễn dịch huỳnh quang cho thấy có ý nghĩa trong những trường hợp không có điều kiện làm phương pháp trực tiếp như nguy cơ gây chảy máu lớn, nhưng có thể gây phản ứng chéo với sốt rét, Toxoplasma, lao kê, thương hàn… (Hiệu giá kháng thể dành cho bệnh do leishmania nội tạng, nhưng không dành cho bệnh do Leishmania spp. da hoặc niêm mạc). Xét nghiệm huyết thanh có thể giúp chẩn đoán bệnh do Leishmaniasp. thể nội tạng, chuẩn độ các kháng thể đối với kháng nguyên Leishmania tái tổ hợp (rk39) hiện diện ở hầu hết các bệnh nhân có khả năng miễn dịch với bệnh do Leishmania nội tạng. Tuy nhiên, những kháng thể có thể không có ở những bệnh nhân HIV/AIDS hoặc những điều kiện suy giảm miễn dịch khác. Xét nghiệm huyết thanh đối với các kháng thể anti-Leishmaina không có ích trong việc chẩn đoán bệnh do Leishmainaspp. thể ngoài da. Chẩn đoán bằng phương pháp sinh học phân tử (PCR) được sử dụng để chẩn đoán xác định và xác định loài chính xác. Xét nghiệm dựa trên phản ứng PCR của dịch chọc hút từ tủy xương, lách, hoặc hạch bạch huyết ở bệnh nhân mắc Leishmaniaspp. thể nội tạng hoặc sinh thiết, chọc hút hoặc các chế phẩm lấy từ tổn thương da giúp chẩn đoán bệnh do Leishmania spp. Xét nghiệm da để phát hiện phản ứng quá mẫn loại chậm với các kháng nguyên Leishmania không có sẵn ở Mỹ. Nó thường có kết quả dương tính ở những bệnh nhân bị bệnh do Leishmania thể da và niêm mạc, nhưng âm tính ở những bệnh nhân có bệnh Leishmaniathể nội tạng hoạt động. ĐIỀU TRỊ & QUẢN LÝ CA BỆNH Tất cả trường hợp bệnh do Leishmaniaspp. nội tạng và ở da và niêm mạc có biểu hiện lâm sàng cần phải được điều trị, trong khi thể bệnh ở da có trường hợp tự khỏi mà không cần điều trị. Tuy nhiên, cần theo dõi chặt chẽ diễn tiến bệnh. Phương pháp điều trị phụ thuộc vào vật chủ và loài ký sinh trùng đơn bào Leishmania spp. mắc phải. Phác đồ điều trị chỉ phù hợp với một loài Leishmania spp., một khu vực địa lý cụ thể. Đối với trẻ em, người cao tuổi, phụ nữ có thai hoặc đang cho con bú, những người bị suy giảm miễn dịch hoặc những người có bệnh nền khác đi kèm,… cần dùng phác đồ thuốc điều trị riêng, chuyên biệt tùy theo tình huống cụ thể. Một số loại thuốc dùng điều trị bệnh nhân nhiễm Leishmania spp.như Pentostam, Amphotericin B, Miltefosine. Dùng các dẫn chất của antimoine như Stibophen, Fuadrin, Neoantimosan, Stibosanune… hoặc Diamidine.Amphotericin B có tác dụng tốtở liều 1 mg/kg/24 giờ, cách nhật 1 ngày, truyền tĩnh mạch trong 1 tháng với tổng liều 450 mg. Đối với thể bệnh ở da, điều trị tại chỗ bằng natri stibogluconat tiêm hoặc paromomycin tại chỗ hoặc liệu pháp nhiệt hoặc áp lạnh; Để điều trị đường toàn thân bệnh do Leishmania pp. ở da, niêm mạc hoặc nội tạng, dùng Amphotericin dạng hạt mỡ đường tĩnh mạch hoặc Miltefosine đường uống. Ngoài ra, chất antimonium Pentavalent (Natri stibogluconate, Meglumine antimoniate) chỉ khi nhiễm các loài Leishmania spp. Hiệu quả điều trị bằng thuốc trên bệnh do Leishmania spp. tùy thuộc vào nhiều yếu tố: ·Hội chứng lâm sàng; ·Loài Leishmania spp. bị nhiễm trên bệnh nhân; ·Vị trí địa lý lưu hành bệnh; ·Khả năng nhạy cảm của ký sinh trùng đơn bào với các loại thuốc chống ký sinh trùng đơn bàoLeishmania spp.; ·Trạng thái miễn dịch của vật chủ với nhiễm Leishmania spp. Các khuyến nghị chi tiết cho việc điều trị có sẵn tại US.CDC: Bệnh do Leishmaniaở da: Điều trị bệnh do Leishmaniaspp. da có thể tại chỗ hoặc hệ thống, tùy thuộc vào tổn thương và ký sinh trùng.Nếu một tổn thương nhỏ, tự lành và không gây ra bởi một loài Leishmania spp. liên quan đến thể bệnh Leishmaniaspp. niêm mạc, nó có thể được theo sát chặt chẽ hơn là điều trị. ·Điều trị tại chỗ: Là một lựa chọn cho tổn thương nhỏ, không biến chứng. Tiêm stibogluconate natri tĩnh mạch đã được sử dụng trong nhiều năm cho thể bệnh da đơn thuần ở châu Âu và châu Á. Hiện không có sẵn điều trị ở Mỹ. Các lựa chọn khác bao gồm trị liệu bằng nhiệt, đòi hỏi một hệ thống chuyên dụng để điều trị và liệu pháp áp lạnh; cả hai đều có thể gây đau và chỉ dùng để điều trị các tổn thương nhỏ. Ngoài ra, paromomycin tại chỗ được sử dụngnhư một loại thuốc mỡ có chứa 15% paromomycin và 12% methylbenzethonium clorid trong dầu thơm màu trắng mềm; ·Trị liệu toàn thân: Sử dụng ở những bệnh nhân có những tiêu chí sau đây: (i) Nhiễm trùng do L. braziliensis hoặc các loài có liên quan gắn liền với bệnh do Leishmaniaspp. niêm mạc; (ii) Bệnh da phức tạp với nhiều tổn thương da, lớn, lan rộng hoặc biến dạng; (iii) Miễn dịch qua trung gian tế bào suy giảm. Tại Mỹ, phương án dùng đường toàn thân gồm liposomal amphotericin B, miltefosine và amphotericin B deoxycholate. Natri stibogluconate hoặc meglumine antimoniate có thể dùng nếu nhiễm trùng ở những nơi không có kháng thuốc. Liposomal amphotericin B và amphotericin B deoxycholate thường được dùng trong các phác đồ dùng cho thể bệnh nội tạng. ·Miltefosine: Có ưu điểm là đường uống, có thể hiệu quả đối với thể bệnh da do L. braziliensis, L. guyanensis và L. panamensis. Miltefosine được dùng theo cân nặng cơ thể: bệnh nhân từ 30-44 kg, uống 50 mg hai lần mỗi ngày trong 28 ngày; ≥ 45 kg, uống 50 mg uống 3 lần mỗi ngày trong 28 ngày. Tác dụng ngoại ý bao gồm buồn nôn, nôn mửa, tăng aminotransferases thoáng qua và chóng mặt. Miltefosine chống chỉ định trong thời kỳ mang thai, phụ nữ trong độ tuổi sinh đẻ đang dùng thuốc này phải sử dụng các biện pháp kiểm soát sinh sản hiệu quả; ·Pentavalent antimonials (sodium stibogluconate, meglumine antimoniate): Chỉ nên dùng nếu nhiễm loài Leishmania spp. nhạy cảm. Meglumine antimoniate được dùng ở Mỹ Latinh. Liều của cả hai đều dựa trên hàm lượng antimon pentavalent - 20 mg/kg IV (cần truyền chậm) hoặc IM một lần/ngày trong 20 ngày. Tác dụng ngoại ý bao gồm buồn nôn, nôn mửa, buồn nôn, tăng amylase và/hoặc men gan, và suy tim (loạn nhịp tim, suy nhược cơ tim, suy tim, thay đổi ECG, ngừng tim). Tỷ lệ tác dụng phụ tăng theo độ tuổi. Thuốc sẽ ngưng lại nếu bệnh nhân bị biến chứng tim mạch do nhiễm độc. ·Các thuốc thay thế gồm nhóm -azole (ví dụ: fluconazole). Fluconazole 200 mg đường uống 1 lần/ngày trong 6 tuần thường không hiệu quả, nhưng thành công đã được báo cáo với liều hàng ngày cao hơn ở một số khu vực. Các nghiên cứu gần đây cho thấy Liposomal amphotericin B với liều tích lũy từ 20-60 mg/kg hoặc miltefosine định lượng theo trọng lượng cơ thể: bệnh nhân 30-44 kg, 50 mg đường uống x 2 lần/ngày trong 28 ngày; ≥ 45 kg, 50 mg đường uống x 3 lần/ngày trong 28 ngày thường có hiệu quả, nhưng dữ liệu còn hạn chế. Tác dụng ngoại ý của miltefosine gồm buồn nôn, nôn, tăng aminotransferase thoáng qua và chóng mặt; Thuốc chống chỉ định trong thời kỳ mang thai vì vậy phụ nữ trong độ tuổi sinh đẻ đang dùng thuốc này phải sử dụng các biện pháp ngừa thai hiệu quả. Về mặt lịch sử, pentavalent antimonials đã được sử dụng nhiều năm trước. Một lựa chọn khác là amphotericin B deoxycholate 0,5 đến 1,0 mg/kg theo đường tĩnh mạch x 1 lần/ngày hoặc hai ngày một lần với tổng liều là từ 20 đến 45 mg/kg. Có thể cần phẫu thuật tái tạo nếu niêm mạc miệng mũi hoặc vòm miệng bị biến dạng, nhưng phẫu thuật nên được trì hoãn 12 giờ sau khi hóa trị thành công để tránh mất mảnh ghép do tái phát. - Bệnh do Leishmaniaspp. thể nội tạng: Liposomal amphotericin B và miltefosine được Cục Quản lý Dược-Thực phẩm Mỹ (US.FDA) phê duyệt để điều trị bệnh do Leishmania nội tạng; các chế phẩm amphotericin liên quan đến lipid khác có thể có hiệu quả nhưng ít được nghiên cứu kỹ hơn.Liều dùng liposomal amphotericin B là: ·Đối với bệnh nhân suy giảm miễn dịch: 3 mg/kg IV một lần/ngày trong 5 ngày và sau đó một lần/ngày vào ngày 14 và 21 (tổng liều 21 mg/kg) ·Đối với bệnh nhân AIDS hoặc các điều kiện miễn dịch khác: 4 mg/kg IV một lần/ngày vào ngày 1 đến 5, 10, 17, 24, 31, và 38 (tổng liều 40 mg/kg) Miltefosine uống, định liều theo trọng lượng cơ thể: bệnh nhân 30-44 kg, 50 mg x 2 lần/ngày trong 28 ngày hoặc đối với bệnh nhân ≥ 45 kg, 50 mg x 3 lần/ngày trong 28 ngày có thể được sử dụng để điều trị bệnh nhân suy giảm miễn dịch nhiễm L. donovani ở Ấn Độ hoặc các khu vực lân cận của Nam Á, > 12 tuổi, nặng > 30 kg và không mang thai hoặc không nuôi có bằng sữa mẹ. Có thể sử dụng thuốc antimonial 5 giá để điều trị bệnh do leishmania nội tạng mắc phải ở Châu Mỹ Latinh hoặc các khu vực khác trên thế giới nơi nhiễm bệnh không kháng lại các loại thuốc này. Liều dùng là 20 mg/kg (dựa trên hàm lượng antimon) IV hoặc IM một lần/ngày trong 28 ngày. Một phương pháp thay thế là amphotericin B deoxycholate 1 mg/kg theo đường tĩnh mạch x 1 lần/ngày trong 15 đến 20 ngày hoặc hai ngày một lần trong tối đa 8 tuần. Sự tái phát phổ biến ở những bệnh nhân AIDS hoặc bệnh nhân có các tình trạng miễn dịch khác. Thuốc kháng retrovirus có thể giúp khôi phục chức năng miễn dịch, làm giảm khả năng tái phát. Dự phòng thứ phát với thuốc kháng leishmania có thể giúp ngăn ngừa tái phát ở bệnh nhân AIDS có CD4 < 200/mcL.Các biện pháp hỗ trợ (như dinh dưỡng thích hợp, truyền máu, kháng sinh đối với nhiễm khuẩn thứ phát) thường là cần thiết cho bệnh nhân bệnh do leishmania nội tạng.
(còn nữa) --> Tiếp theo phần 3
TÀI LIỆU THAM KHẢO 1.Aronson N, Herwaldt BL, Libman M, et al: Diagnosis and treatment of leishmaniasis: Clinical Practice Guidelines by the Infectious Diseases Society of America (IDSA) and the American Society of Tropical Medicine and Hygiene (ASTMH). Clin Infect Dis 63 (12):e202-e264, 2016. 2.Centers for Disease Control and Prevention (CDC): Resources for Health Professionals. 3.Steverding D. The history of leishmaniasis. Parasit Vectors. 2017 Feb 15;10(1):82. 4.Zink AR, Spigelman M, Schraut B, Greenblatt CL, Nerlich AG, Donoghue HD. Leishmaniasis in ancient Egypt and Upper nubia. Emerg Infect Dis. 2006 Oct;12(10):1616-7. 5.Claborn DM. The biology and control of leishmaniasis vectors. J Glob Infect Dis. 2010 May;2(2):127-34. 6.Handler MZ, Patel PA, Kapila R, Al-Qubati Y, Schwartz RA. Cutaneous and mucocutaneous leishmaniasis: Differential diagnosis, diagnosis, histopathology, and management. J Am Acad Dermatol. 2015 Dec;73(6):911-26; 927-8. 7.Torres-Guerrero E, Quintanilla-Cedillo MR, Ruiz-Esmenjaud J, Arenas R. Leishmaniasis: a review. F1000Res. 2017;6:750. 8.Handman E, Bullen DV. Interaction of Leishmania with the host macrophage. Trends Parasitol. 2002 Aug;18(8):332-4. 9.Rogers ME, Chance ML, Bates PA. The role of promastigote secretory gel in the origin and transmission of the infective stage of Leishmania mexicana by the sandfly Lutzomyia longipalpis. Parasitology. 2002 May;124(Pt 5):495-507. 10.de Vries HJ, Reedijk SH, Schallig HD. Cutaneous leishmaniasis: recent developments in diagnosis and management. Am J Clin Dermatol. 2015 Apr;16(2):99-109. 11.Hosseinzadeh M, Omidifar N, Lohrasb MH. Use of fine needle aspiration cytology in the diagnosis of cutaneous leishmaniasis: a comparison with the conventional scraping method. Trop Doct. 2012 Apr;42(2):112-3. 12.Sousa AQ, Pompeu MM, Frutuoso MS, Lima JW, Tinel JM, Pearson RD. Press imprint smear: a rapid, simple, and cheap method for the diagnosis of cutaneous leishmaniasis caused by Leishmania (Viannia) braziliensis. Am J Trop Med Hyg. 2014 Nov;91(5):905-7. 13.Tofighi Naeem A, Mahmoudi S, Saboui F, Hajjaran H, Pourakbari B, Mohebali M, Zarkesh MR, Mamishi S. Clinical Features and Laboratory Findings of Visceral Leishmaniasis in Children Referred To Children Medical Center Hospital, Tehran, Iran during 2004-2011. Iran J Parasitol. 2014 Mar;9(1):1-5. 14.Amato VS, Tuon FF, Siqueira AM, Nicodemo AC, Neto VA. Treatment of mucosal leishmaniasis in Latin America: systematic review. Am J Trop Med Hyg. 2007 Aug;77(2):266-74. 15.Moore EM, Lockwood DN. Treatment of visceral leishmaniasis. J Glob Infect Dis. 2010 May;2(2):151-8. 16.Alvar J, Vélez ID, Bern C, Herrero M, Desjeux P, Cano J, Jannin J, den Boer M., WHO Leishmaniasis Control Team. Leishmaniasis worldwide and global estimates of its incidence. PLoS one. 2012;7(5):e35671. 17.Berman JD, Badaro R, Thakur CP, Wasunna KM, Behbehani K, Davidson R, Kuzoe F, Pang L, Weerasuriya K, Bryceson AD. Efficacy and safety of liposomal amphotericin B (AmBisome) for visceral leishmaniasis in endemic developing countries. Bull World Health Organ. 1998;76(1):25-32. 18.Sundar S, Jha TK, Thakur CP, Engel J, Sindermann H, Fischer C, Junge K, Bryceson A, Berman J. Oral miltefosine for Indian visceral leishmaniasis. N Engl J Med. 2002 Nov 28;347(22):173 19.Abongomera C, Gatluak F, Buyze J, Ritmeijer K. A Comparison of the Effectiveness of Sodium Stibogluconate Monotherapy to Sodium Stibogluconate and Paromomycin Combination for the Treatment of Severe Post Kala Azar Dermal Leishmaniasis in South Sudan - A Retrospective Cohort Study. PLoS one. 2016;11(9):e0163047. 20.Abongomera C, Diro E, Vogt F, Tsoumanis A, Mekonnen Z, Admassu H, Colebunders R, Mohammed R, Ritmeijer K, van Griensven J. The Risk and Predictors of Visceral Leishmaniasis Relapse in Human Immunodeficiency Virus-Coinfected Patients in Ethiopia: A Retrospective Cohort Study. Clin Infect Dis. 2017 Oct 30;65(10):1703-1710.
|

