|
Thông tin cập nhật về bệnh sán lá gan lớn Fascioliasis trên thế giới
Hiệu quả của albendazole và triclabendazole lên cầu nối vi vỏ colchicin của F. hepatica
Albendazole (ABZ) và các chất chuyển hóa sulfoxide (SX), sulfone (SO) ức chế quá trình hình thành cầu nối trong cấu trúc vi vỏ 3H-colchicine, đây là một cầu nối có tính bền vững trong hỗ trợ cho cấu trúc vi quản đính với một số thành phần cơ thể của SLGL Fasciola hepatica. Về thực nghiệm, hiệu quả của hợp chất SX mạnh hơn, lớn hơn ABZ và lớn hơn SO. Nhóm thuốc benzimidazoles (gồm cambendazole, parbendazole, oxibendazole và mebendazole), khi thử nghiệm ở nồng độ 10 microM, cũng cho phép ức chế cầu nối của sán. Tuy nhiên, một tiềm năng lớn của nhóm thuốc diệt sán benzimidazole mới này là thuốc triclabendazole (TCZ), lại không tác động lên cầu nối colchicine với chất đồng nhất của F. hepatica mà theo một cơ chế khác. Khi sán còn nguyên vẹn, người ta cho tiếp xúc, thử nghiệm in vitro với nồng độ 0 (-5) M SX trong thời gian 5 phút, sau đó cầu nối 3H-colchicine với chất đồng nhất của sán giảm đi một cách đáng kể. Tuy nhiên, với ABZ thì sán lại phục hồi trong vòng 12-24 giờ sau khi xử lý trên cừu bằng ABZ và không có giảm cầu nối colchicine đáng kể và cũng đã cho thấy một vài tương tác thuốc với vi quản trên in vivo. Nhìn chung, thuốc ABZ, SX và SO có hiệu quả ngăn cản quá trình hình thành tạo phôi của trứng sán ở liều thấp 0.01 microM, nhưng TCZ không tác động ở nồng độ cao 10 microM. Kết quả cho thấy ABZ thể hiện phần nào trong tác động của chúng lên quá trình trưởng thành của sán nhờ quá trình tương tác thuốc với cấu trúc vi quản.
So sánh hiệu quả Albendazole, Fenbendazole và Triclabendazole trên F.hepaticaCông trình nghiên cứu này mô tả so sánh giữa Albendazole (ABZ), Fenbendazole (FBZ) và Triclabendazole (TCZ) trong cơ chế tác động xuyên thấu cấu trúc vi vỏ của sán Fasciola hepatica trưởng thành và ảnh hưởng một số thành phần lý hóa trong môi trường ủ bệnh có mật lên thuốc trong quá trình khuyếch tán thuốc. Dữ liệu thu nhận được từ nghiên cứu động lực khuyếch tán xuyên cấu trúc vi vỏ (trans-tegumental diffusion kinetic) có sự trợ giúp của thành phần bổ sung đi kèm với lipid là nước [lipid-to-water coefficients (octanol-water)] đối với nhóm thuốc benzimidazole (BZD) được thử nghiệm. Sán lá gan F. hepatica 16 tuần tuổi được thu thập từ các con cừu nhiễm tự nhiên chưa điều trị thuốc gì. Những con sán được ủ ở nhiệt độ 37°C trong thời gian trên 60-90 phút trong môi trường có pH 7.4 và tỷ lệ giữa mật bò với dung dịch đệm Krebs' Ringer Tris (KRT) buffer khác nhau (100, 75, 50, 25 và 0% mật bò) chứa các thuốc. Hoặc là ABZ, FBZhoặc TCZ ở các nồng độ cuối cùnglà 5 nmol/ml. Sau thời gian ủ bệnh kết thúc, các con sán trong gan được xử lý hóa học và phân tích bằng kỹ thuật sắc ký lỏng cao áp (HPLC) để đo nồng độ thuốc bên trong ký sinh trùng sán lá này. Ngoài ra, tỷ lệ chia giữa octanol-nước cho mỗi phân tử được tính (xem như là một chỉ số ưa lipid của thuốc sử dụng pha đảo của HPLC. Các phân tử của 3 BZD được hồi phục từ các con F. hepatica ở tất cả môi trường ủ bệnh được kiểm định chi tiết nhằm so sánh. Sự khuyếch tán xuyên vi vỏ phân tử ưa lipid của ABZ và FBZ (cao hơn giá trị PC) có xu hướng lớn hơn của TCZ đã qua kiểm tra. Một điều thú vị, hấp thu ABZ do sán lá gan cao hơn do TCZ một cách có ý nghĩa và TCZ là hợp chất diệt sán phổ rộng hơn BZD.
Mô hình hấp thụ khác biệt này có thể lộ ra một vấn đề cần quan tâm bấy lâu nay nhằm giải thích cho quy trình sán lá gan lớn kháng thuốc TCZ. Nồng độ thuốc được đo trong ký sinh trùng thấp hơn trong môi trường ủ thực nghiệm mà có nồng độ mật bò cao nhất. Cùng với ý nghĩa đó, thử nghiệm này cho thấy đường vào của thuốc đến đích của ký sinh trùng sán lá không những chỉ phụ thuộc vào chên lệch nồng độ, vào tính ái lipid của các phân tử và bề mặt hấp thụ (lipophilicity of the molecule and absorption surface), mà còn bị ảnh hưởng từ thành phần lý hóa trong môi trường xung quanh mà con sán tồn tại lúc đó. 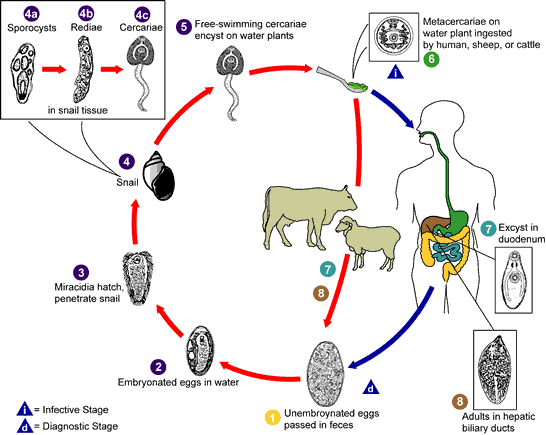 | Chu kỳ phát triển của Sán lá gan |
Triclabendazole: Một công cụ “mới” làm sáng tỏ một cơ chế “cũ” Triclabendazole (TCZ) được giới thiệu lần đầu tiên vào đầu những năm 1980 để điều trị nhiễm ký sinh trùng Fasciola hepatica trên vật nuôi và một số gia súc. Do hoạt tính của thuốc cao trên các sán lá gan lớn chưa trưởng thành, thuốc TCZ này trở thành một trong những thuốc chính yếu trong điều trị sán trên thị trường vào thời điểm đó. Song gần đây, TCZ được sử dụng điều trị sán lá gan lớn (SLGL) ở người và đến nay gần 15 năm sau TCZ đã là thuốc được lựa chọn đầu tay của bệnh nhân sán lá gan lớn. Kháng thuốc TCZ được báo cáo lần đầu tiên năm1995 ở một vài nơi bệnh lưu hành ở Úc và từ đó nó được quan tâm và xuất hiện và được một số tác giả báo cáo nhiều quốc gia ở châu Âu. Song song với sự lan rộng của kháng thuốc, thì có tăng đáng kể về tỷ lệ bệnh SLGL, trong đó có sự góp phần của thay đổi thời tiết, khí hậu. Do đó, người nông dân, nhất là các chủ trang trại gia súc đang phải đối mặt với với một viễn cảnh đầy báo động, thiệt hại rất lớn đến nền kinh tế công nghiệp chăn nuôi. Mục đích chính là để đánh giá những hiểu biết gần đây về cơ chế tác dụng của TCZ chống lại SLGL và cơ chế SLGL làm thế nào tạo ra kháng thuốc kháng thuốc như vậy. Việc sử dụng TCZ chống lại bệnh SLGL ở người và động vật đã được kết luận và mở ra hướng đi mới giải thích cơ chế kháng thuốc bằng những nghiên cứu chi tiết trên thế giới. Những lỗ hỗng về kiến thức cập nhật về các khía cạnh khác nhau là rất lớn và đóng vai trò định hướng các nghiên cứu trong tương lai cho lĩnh vực này. Chuyển dạng sinh học và khuyếch tán thuốc triclabendazole-một so sánh trên thuốc gốc và chất chuyển hóa oxy hóa vào trong cơ thể F.hepatica Triclabendazole (TCZ) là một hợp chất benzimidazole halogen hóa diệt sán lá được dùng phổ biến trong lĩnh vực thú y. Hoạt tính tác động mạnh trên sán trưởng thành và chưa trưởng thành sán lá gan Fasciola hepatica. Chất chuyển hóa ở gạn gắn kết và ở dạng tự do TCZ được xác định cơ chế chuyển dạng và tác dụng trên những con cừu được điều trị thuốc này. Mục đích nghiên cứu thực nghiệm là để kiểm tra đặc tính trên mô hình in vitro của chuyển dạng sinh học của TCZ cả những vật chủ động vật (tiểu bào tử của gan cừu) và ký sinh trùng đích (các chế phẩm tiểu bào tử F. hepatica); so sánh với khuyếch tán ex vivo của TCZ gốc và chất chuyển hóa oxy của chúng là sulphoxide TCZ [TCZSO], TCZ sulphone [TCZSO2], dẫn suất TCZ-hydroxy vào trong sán F. hepatica. Thêm vào đó, thành phần gắn kết octanol-nước đối với TCZ và tất cả chất chuyển hóa của chúng được đánh giá như là một chỉ số liên quan giữa tính ưa lipid và khuyếch tán vào trong đích của ký sinh trùng, quá trình và sơ bộ kết quả ban đầu được tóm lược như sau: 1. Nồng độ thuốc hoặc chất chuyển hóa được định lượng, tính thông qua kỹ thuật của sắc ký lỏng cao áp (HPLC) sau khi mẫu được rửa sạch và tách chiết dựa vào hóa chất môi trường được pha loãng. 2. Tiểu bào tử gan của cừu sẽ chuyển hóa TCZ thành những chất sulphoxide vàsulfone sau 30 phút ủ với gan. Tỷ lệ hóa TCZ sulphoxidate trên gan cao có ý nghĩa thống kê(p<0.01) hơn là sulfon hóa của TCZSO. 3. Ký sinh trùng được oxy hóa TCZ thành những chất chuyển hóa sulphoxide sau 60 phút ủ ở tỷ lệ 0.09 nmol min−1 mg protein−1 4. TCZ và tất cả sản phẩm được oxy hóa chuyển hóa được hồi phục lại từ F. hepatica sau 15 phút sau khi ủ theo ex vivo trong một môi trường có thuốc đệm Kreb's Ringer Tris buffer. Tuy nhiên, sự khuyếch tán của dẫn suất hydroxy vào trong sán là thấp hơn hàm lượng mà TCZ, TCZSO và TCZSO2 được quan sát. Có mối tương quan rất chặt chẽ (r = 0.82) giữa ưa lipid của thuốc (biểu thị qua thành phần kết dính giữa octanol-nước) và sinh khả dụng của thuốc được đo trong cơ thể sán. 5. Không giống như mô hình hấp thu trước đây được quan sát ở thuốc albendazole, thuốc gốc TCZ và các dẫn suất chuyển sulphoxide và sulphone cho thấy chúng có khả năng tương tự xuyên thấu vào trong cơ thể sán. 6. Những hiểu biết về liên quan giữa chuyển hóa TCZ, tiềm năng dược lý tương đốicủa các sản phẩm chuyển hóavà khả năng đạt đến đích ký sinh trùng có thể là hoạt tính chủ yếu lên cấu trúc vi vỏ của sán, đặc biệt khi sán đề kháng TCZ được phân lập rõ ràng trên thực địa. Đáp ứng của hai phân lập F.hepatica với thuốc Triclabendazole trên mô hình thử nghiệm in vivo và in vitro Trong nghiên cứu này, các nhà khoa học đã khảo sát tính nhạy cảm của hai phân lập của loài sán lá gan lớn Fasciola hepatica (phân lập Fairhurst và Oberon) khi điều trị chúng bằng thuốc Triclabendazole (TCZ) cả trên in vivo và in vitro. Phân lập Fairhurst có nguồn gốc từ Anh, nhưng có tồn tại ở Australia nên cũng được đua vào nghiên cứu này và phân lập Oberon có nguồn gốc từ Australia. Triclabendazole (TCZ) có hiệu lực rất cao chống lại phân lập Fairhurst. Trên cừu (liều 10mg/kg), hiệu quả đạt từ 78.4% (theo dõi ở thời điểm 2 tuần sau nhiễm) đến 98.5% (ở thời điểm 6 tuần sau nhiễm). Trên gia súc khác (liều 12mg/kg) hiệu quả đạt được 89% (ở 2 tuần sau nhiễm) và 100% (ở thời điểm 12 tuần sau nhiễm). Ngược laị, đối với phân lập Oberon, thuốc TCZ chỉ đạt hiệu quả 0% chống lại những con sán lá gan lớn 2 tuần tuổi trên cừu (liều 10mg/kg) và chỉ 5% chống lại những con sán 4 tuần tuổi. Sự thay đổi bề mặt cấu trúc vi vỏ của sán từ hai phân lập trên khi cho thuốc tác động được đánh giá, khảo sát bằng kính hiển vi điện tử (SEM-scanning electron microscopy) theo dõi sau điều trị trên in vitro đối với các chuyển hóa của TCZ là sulphoxide trong 24 giờ (nồng độ 15 và 50 g/ml). Sự phá hủy cấu trúc ở dạng tạo nốt phỏng và sưng phồng, rồi tạo các rãnh cắt trên cấu trúc vi vỏ ở phân lập Fairhurst lớn hơn so với phân lập Oberon. Thay đổi bề mặt nói chung rất nghiêm trọng ở vùng trước cơ thể hơn vùng sau của sán và phần lưng cũng bị ảnh hưởng năng hơn phần phần bụng. Sự phá hủy càng nặng nếu nồng độ thuốc cho tiếp xúc càng cao đối với cả hai phân lập. Dữ liệu về hình thể học được phân tích đồng thời với dữ liệu về hiệu quả thuốc. Kết quả quan sát đã chỉ ra phân lập Fairhurst của F. hepatica nhạy cảm với thuốc TCZ trong khi phân lập Oberon lại tỏ ra “chịu đựng” khá tốt dưới áp lực nồng độ thuốc tăng cao dần hoặc chỉ bị ảnh hưởng ít không đáng kể.
|

