QUÁ TRÌNH GÂY UNG THƯ DO SÁN LÁ GAN NHỎ C. sinensis
Mối liên quan giữa C. sinensis và ung thư đường mật ở người
Trường hợp ung thư đường mật (CCA) đầu tiên liên quan đến C. sinensis được báo cáo tại Trung Quốc vào năm 1919. Kể từ đó, nhiều nghiên cứu đã báo cáo về mối tương quan nhân quả giữa CCA và C. sinensis. Tại Hàn Quốc, vào năm 1948, ông Ju Shik Lee, một cán bộ thuộc Bộ Y tế và Nhân sinh đã khẳng định rằng có rất nhiều bệnh nhân ung thư gan kèm theo các bệnh lý liên quan như vàng da và cổ trướng tại Busan. Qua điều tra những bệnh nhân này, ông nhận thấy nhiều người trong số họ bị nhiễm C. sinensis rất nặng. Một số cuộc khảo sát và dữ liệu bệnh viện đã xác nhận rằng C. sinensis lưu hành rất cao với tỷ lệ dương tính với trứng sán từ 50-70% tại Busan và các địa phương lân cận dọc theo lưu vực sông Nakdong.
Tuy nhiên, công việc của ông đã bị gián đoạn bởi Chiến tranh Triều Tiên vào năm 1950 và không thể tiếp tục sau đó. Những phát hiện của ông đã gợi ý về mối liên quan tiềm tàng giữa bệnh SLGN và CCA tại các vùng lưu hành bệnhSLGN.
Các nghiên cứu dịch tễ học
Có nhiều báo cáo từ các nghiên cứu ca bệnh tại bệnh viện và nghiên cứu dịch tễ ghi nhận mối tương quan giữa bệnh SLGN và CCA. Tại Hồng Kông, các nghiên cứu dựa trên loạt ca khám nghiệm tử thi trong những năm 1950 và 1960 đã mô tả những quan sát bệnh lý về CCA không kèm xơ gan có liên quan đến C. sinensis. Các bài báo này báo cáo tỷ lệ mắc SLGN cao tại Hồng Kông và mô tả các đặc điểm bệnh lý của đường mật trong gan trong các trường hợp CCA kèm nhiễm SLGN. Khối u lan rộng dọc theo ống mật trong gan gây tắc mật. Về mặt mô bệnh học, các ống mật bị giãn với tình trạng tăng sản dạng tuyến của biểu mô và xơ hóa quanh ống mật.
Hầu hết các trường hợp đều cho thấy nhiều khối u di căn. Những nghiên cứu loạt ca bệnh này đã mô tả các phát hiện khám nghiệm tử thi của bệnh nhân CCA, qua đó làm rõ bệnh lý gan trong nhiễm SLGNở người và gợi ý mối quan hệ nhân quả với bệnh SLGN tại Hồng Kông.Tại Hàn Quốc, Kim và cộng sự đã so sánh dữ liệu bệnh viện từ các bệnh nhân ung thư nguyên phát và CCA tại Seoul và Busan, trong đó Seoul là vùng không lưu hành nhưng Busan là vùng lưu hành SLGN. Tỷ lệ ung thư biểu mô gan nguyên phát là 26,7% ở Seoul và 27,5% ở Busan, cho thấy không có sự khác biệt đáng kể. Tuy nhiên, CCA chiếm 8,6% các trường hợp ung thư gan nguyên phát ở Seoul nhưng chiếm tới 19,3% ở Busan, đây là một sự khác biệt có ý nghĩa. Tỷ lệ hiện mắc SLGN là 38,9% ở bệnh nhân CCA, so với 8,0% ở bệnh nhân ung thư biểu mô tế bào gan (hepatocellular carcinoma HCA). Nghiên cứu cho thấy tỷ lệ CCA ở vùng lưu hành SLGNcao hơn so với vùng không lưu hành, cũng như tỷ lệ nhiễm SLGN ở bệnh nhân CCA cao hơn so với bệnh nhân HCA. Một nghiên cứu khác tại Busan đã chứng minh rằng nguy cơ tương đối của bệnh SLGNđối với CCA cao gấp 5 lần so với HCA. Hai nghiên cứu lâm sàng này đã mô tả một mối liên quan có khả năng rất cao giữa CCA và bệnh SLGN tại Hàn Quốc.
Sau đó, Shin và cộng sự đã điều tra mối tương quan dịch tễ học giữa CCA và bệnh SLGN tại Busan, gợi ý nguy cơ tương đối là 2,7 (95%CI: 1,1-6,3) đối với CCA do nhiễm SLGN. Shin và cộng sự cũng ước tính tỷ số chênh (OR) của CCA do bệnh SLGN là 4,7 (95% CI: 2,2-9,8), và nhận thấy khoảng 10% các trường hợp CCA tại Hàn Quốc có liên quan đến nhiễm SLGN mạn tính. Một phân tích tổng hợp đã xác định các yếu tố nguy cơ đối với CCA, tiết lộ rằng SLGN, kểcả C. sinensis và O. viverrini), virus viêm gan B và virus viêm gan C có nguy cơ tương đối lần lượt là 4,8 lần (2,8–8,4), 2,6 (1,5–4,6) và 1,8 (1,4-2,4). Nghiên cứu cũng chứng minh rằng tiền sử đã từng nhiễm SLGN là một yếu tố nguy cơ đáng kể của CCA, bên cạnh tình trạng nhiễm bệnh hiện tại.
Lim và cộng sự (2006) đã khảo sát tỷ lệ hiện mắc SLGNtại các khu vực không lưu hành (2,1%), lưu hành nhẹ (7,8%) và lưu hành vừa (31,3%). Họ đã so sánh tỷ lệ tử vong và tỷ lệ mắc mới ung thư đường mật (CCA) tại các vùng này bằng cách sử dụng dữ liệu tử vong quốc gia và cơ sở dữ liệu đăng ký ung thư tại Hàn Quốc. Tỷ lệ tử vong do CCA chuẩn hóa theo độ tuổi lần lượt là 1,2; 1,1 và 2,6/100.000 dân; trong khi tỷ lệ mắc mới CCA tương ứng là 0,3; 1,8 và 5,5/100.000 dân tại các khu vực không lưu hành, lưu hành nhẹ và lưu hành vừa. Tỷ số chênh (OR) của bệnh SLGNlà 14,7 (95% CI: 7,90-25,00) ở khu vực lưu hành vừa so với khu vực không lưu hành. Tỷ lệ CCA trong tổng số các ca ung thư gan nguyên phát lần lượt là 1,4%, 8,9% và 13,2% tương ứng với các mức độ lưu hành nêu trên.
Choi và cộng sự đã thu thập dữ liệu từ các bệnh nhân mắc CCA kèm bệnh SLGNvà phân tích hình ảnh học của gan. Họ quan sát thấy mối tương quan chặt chẽ về mặt căn nguyên giữa SLGN và CCA, đồng thời xem xét dữ liệu chẩn đoán hình ảnh của bệnh nhân. Hầu hết bệnh nhân SLGN đều có tình trạng giãn đường mật trong gan và trong các ca CCA, có sự giãn đường mật ở đoạn xa so với khối u. Sự kết hợp của các đặc điểm hình ảnh này được coi là dấu hiệu đặc trưng (pathognomonic) cho ung thư đường mật liên quan đến SLGN.Trong một nghiên cứu sau đó, phân tích hồi cứu dữ liệu lâm sàng từ một bệnh viện tuyến cuối tại Seoul đã xác nhận rằng hình ảnh học đặc trưng của C. sinensis, tiền sử ăn cá nước ngọt sống và xét nghiệm huyết thanh dương tính là những yếu tố nguy cơ đáng kể của CCA.
Tỷ số chênh cho các yếu tố nguy cơ này lần lượt là OR: 8,615 (95%CI: 5,045-16,062); OR: 2,385 (95% CI: 1,527–3,832); và OR: 2,272 (95% CI: 1,147-4,811). Một nghiên cứu lâm sàng khác tại một bệnh viện tuyến cuối ở Hàn Quốc cũng xác định SLGNlà một trong những yếu tố nguy cơ đáng kể đối với CCA trong gan với OR là 13,6. Những phát hiện này trên bệnh nhân CCA đã cung cấp bằng chứng rõ ràng về mối tương quan nhân quả đáng kể giữa bệnh SLGN và CCA trong quần thể người, góp phần vào việc Cơ quan Nghiên cứu Ung thư Quốc tế (IARC) tái phân loại C. sinensis từ tác nhân gây ung thư Nhóm 2A lên Nhóm 1 (tác nhân gây ung thư sinh học) vào năm 2009.
Tại Trung Quốc, Shi và cộng sự đã phân tích 20 bệnh nhân ung thư gan nguyên phát, bao gồm 8 ca CCA và 11 ca ung thư biểu mô tế bào gan (HCA). Trong số 8 bệnh nhân CCA, có 7 người nhiễm C. sinensis và 2 người đồng nhiễm virus viêm gan B. Trong 11 bệnh nhân HCA, có 10 người nhiễm C. sinensis và 4 người đồng nhiễm virus viêm gan B. Họ gợi ý rằng việc đồng nhiễm C. sinensis và virus viêm gan B dẫn đến nguy cơ cao mắc cả CCA và HCA. Shin và cộng sự cũng đề xuất rằng virus viêm gan B và C có khả năng gây ung thư liên quan đến CCA. Hiệu ứng gây ung thư hiệp đồng giữa C. sinensis và các virus viêm gan hoặc các mầm bệnh vi sinh khác có thể là hướng cần nghiên cứu thêm. Một phân tích tổng hợp tại Trung Quốc báo cáo OR của các loại sán lá gan ở người đối với CCA là: 4,49 (95% CI: 3,43–5,87, P < 0,001) đối với C. sinensis và 3,69 đối với O. viverrini. OR của bệnh SLGNđi kèm sỏi mật là 3,69. Các nghiên cứu này được tóm tắt tại Bảng 1
Bảng 1. Các nghiên cứu về bệnh SLGN do Clonorchissinensis ở người và ung thư đường mật (CCA)
Các mô hình động vật
Nhiều thử nghiệm trên động vật đã được thực hiện nhằm nghiên cứu về bệnh lý miễn dịch, tương tác giữa vật chủ và ký sinh trùng, các biến đổi di truyền và bệnh sinh của CCA do nhiễm C. sinensis. Ung thư đường mật do C. sinensis đặc trưng bởi quá trình tái cấu trúc quá mức và liên tục của các tế bào đường mật thông qua sự kích thích và tổn thương kéo dài do giun sán gây ra.
Vi môi trường gan liên quan đến khối u bao gồm các tế bào gan, tế bào nội mô xoang gan, tế bào hình sao, tế bào biểu mô đường mật, tế bào Kupffer và các tế bào miễn dịch được huy động, bao gồm cả đại thực bào có nguồn gốc từ tủy xương. Như đã mô tả ở trên, sán trưởng thành C. sinensis gây ra các tổn thương cơ học và viêm nhiễm lên thành ống mật, dẫn đến tăng sản dạng tuyến và chuyển sản các tế bào tiết chất nhầy ở niêm mạc đường mật.
Bên cạnh các phát hiện về mô bệnh học này, những thay đổi của biểu mô đường mật nhằm đáp ứng với các kích thích trong bệnh SLGNcấp tính và mãn tính bao gồm sự thâm nhiễm của các tế bào Kupffer, đại thực bào và sự hình thành nang ở chuột.
Những thay đổi bệnh lý này ở chuột có xu hướng tương quan với thời gian nhiễm C. sinensis, cường độ nhiễm sán và tính cảm nhiễm của vật chủ. Để nhận diện tác nhân gây bệnh, thụ thể Toll-like 2 (TLR2) và TLR4 được ghi nhận là tăng biểu hiện trong mô hình chuột nhiễm C. sinensis. Sự tăng biểu hiện TLR4 đã kích thích bài tiết yếu tố hoại tử u (Tumor Necrosis Factor alpha-TNF-α) trong các tế bào biểu mô đường mật chuột khi được kích thích bởi sản phẩm bài tiết-ngoại tiết (excretory-secretory product-ESP).Kim và cộng sự báo cáo rằng các tế bào Kupffer đóng vai trò như những tế bào trình diện kháng nguyên và tăng gấp 70 lần trong giai đoạn nhiễm C. sinensis sơ cấp. Các tế bào Kupffer thu hồi được đã sản sinh mức độ cytokine cao hơn đáng kể, bao gồm TNF-α, interleukin (IL)-6, IL-10 và IL-13, trên dòng chuột FVB nhiễm C. sinensis.
Tuy nhiên, ảnh hưởng từ việc sản sinh TNF liên tục bởi các tế bào Kupffer và tế bào biểu mô đường mật đối với tổn thương gan mãn tính và nồng độ cao các gốc oxy hóa tự do (reactive oxygen species - ROS) vẫn chưa được làm rõ. Các tế bào Kupffer tập trung ở các mô quanh ống mật và gần các tĩnh mạch.
Ngoài ra, gan của chuột bị xơ gan cho thấy sự thâm nhiễm của các tế bào Kupffer xung quanh vùng cửa. Số lượng tế bào Kupffer được huy động tăng lên tại các khu vực đặc trưng bởi sự tái cấu trúc mô trong giai đoạn xơ gan của quá trình nhiễm bệnh. Tế bào Kupffer được kích hoạt bởi các thành phần khác nhau và có thể biệt hóa thành đại thực bào M1 (điển hình) hoặc M2 (thay thế) tại gan.
Đại thực bào M1 ức chế sự phát triển của khối u, trong khi đại thực bào M2 góp phần vào sự tiến triển của ung thư. Giai đoạn xơ hóa và xơ gan sau khi nhiễm C. sinensis làm tăng rõ rệt tỷ lệ đại thực bào sản sinh Arg-1 (kiểu hình M2), giúp điều hòa quá trình xơ hóa và sửa chữa mô, đồng thời thúc đẩy sự chuyển đổi ác tính của các tế bào đường mật.
Các loài động vật vật chủ khác nhau biểu hiện tính cảm nhiễm khác nhau đối với việc nhiễm C. sinensis, nhưng chuột hamster, chuột guinea pig và thỏ được coi là những vật chủ thí nghiệm tốt trong phòng thí nghiệm. Trong số đó, chuột hamster vàng Syrian là mô hình phù hợp nhất cho các nghiên cứu về ung thư đường mật (CCA).
Các nghiên cứu trước đây đã báo cáo rằng tình trạng nhiễm C. sinensis đóng vai trò là tác nhân thúc đẩyvà cần có một tác nhân khởi đầu, chẳng hạn như N-nitrosodimethylamine (NDMA) để gây ra CCA. Các chất gây ung thư, bao gồm NMDA, khởi phát quá trình tạo u thông qua quá trình methyl hóa DNA và gây ra tác động độc hại di truyền, dẫn đến những thay đổi cấu trúc trong DNA.
Không quan sát thấy những thay đổi tân sinh rõ rệt của CCA trên các dòng chuột BALB/c, ICR, B6 và C3H/He khi nhiễm C. sinensis và tiếp xúc với NDMA. Thay vì CCA, chuột C3H/He phát triển tình trạng xơ hóa lan tỏa khi được gây nhiễm đồng thời với C. sinensis, NDMA và dicyclanil. Điều thú vị là các u tuyến (adenoma) chỉ phát triển ở dòng chuột FVB, đi kèm với sự giãn nở dạng nang của ống mật bị nhiễm bệnh. Không có loài động vật nào khác phát triển CCA thông qua việc gây nhiễm thực nghiệm với C. sinensis
Đặc điểm của mô hình chuột Hamster
Các tổn thương dạng khối (Mass-Forming Lesions - MFLs) là phát hiện bệnh lý chính của ung thư đường mật (CCA) được gây ra bởi C. sinensis và NDMA trên mô hình chuột hamster vàng Syrian, với tỷ lệ hiện mắc MFLs là 100% ở nhóm chuột hamster nhiễm C. sinensis + NDMA. Các giai đoạn tiến triển mô học của CCA xảy ra tuần tự từ CCA biệt hóa tốt, sau đó là CCA biệt hóa kém theo thời gian, bắt đầu từ tuần thứ 8 sau khi nhiễm bệnh.
Một nghiên cứu khác sử dụng mô hình chuột hamster vàng Syrian đã báo cáo rằng các kích thích cơ học và hóa học liên tục bởi C. sinensis và NDMA làm tăng biểu hiện các gen quan trọng trong ung thư, bao gồm PSMD10, CDK4 và PCNA, đồng thời làm giảm biểu hiện gen ức chế khối u TP53, cũng như protein RB, caspase-9 và BAX. Sự giảm biểu hiện của BAX và caspase-9 có thể tạo điều kiện thuận lợi hơn cho sự sống sót của các tế bào đã bị biến đổi có DNA bị biến tính và những tế bào đang tăng sinh không kiểm soát để hình thành khối CCA.
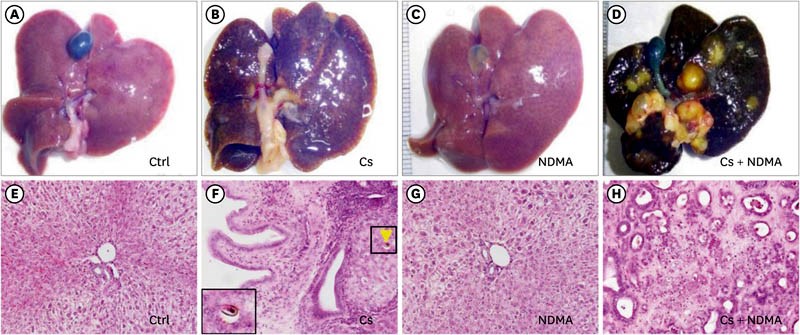
Hình 6. Quá trình sinh ung thư thực nghiệm trên chuột hamster vàng Syrian được gây ra bởi Cs và NDMA. Hình thái đại thể của gan: Nhóm chứng (A), chỉ nhiễm Cs (B), chỉ dùng NDMA (C), Cs + NDMA (D). Mô bệnh học của gan: Nhóm chứng (E), chỉ nhiễm Cs, các khung đánh dấu trứng sán trong ống mật (F), chỉ dùng NDMA (G), Cs + NDMA (H). Độ phóng đại gốc ×200 (E-H), nhuộm hematoxylin-eosin. Được trích dẫn từ tài liệu tham khảo 71 (Ctrl = nhóm chứng, Cs = C. sinensis, NDMA = N-nitrosodimethylamine.
Sự quá biểu hiện của PCNA có thể được phát hiện trong mô u như một chỉ điểm của CCA trong hoại tử u. Các thí nghiệm trên động vật về quá trình sinh ung thư được tóm tắt trong Bảng 2.
Bảng 2. Các nghiên cứu trên động vật về sán lá gan nhỏ C. sinensis và un thư CCA
Còn nữa --> Tiếp theo Phần 4
TS.BS. Huỳnh Hồng Quang & CN. Nguyễn Thái Hoàng
Viện Sốt rét-KST-CT Quy Nhơn