Mặc dù hiện nay trị liệu phối hợp chống kháng có gốc Artemisinine (ACTs_Artemisinine-based Cobination Therapy) đang được khuyến cáo sử dụng điều trị sốt rét kháng thuốc trên phạm vi toàn cầu, tuy nhiên các nhà sản xuất đã dự tính một sản phẩm thuốc sốt rét mới thay thế nếu ACTs bị kháng bởi P.falciparum. Sản phẩm mới này có mã số OZ 277/Rbx 11160 là một chất tổng hợp có cấu trúc tương tự Artemisinin được xem như vũ khí chính trong cuộc chiến chống lại bệnh sốt rét đa kháng thuốc và bước đột phá lớn nhất trong điều trị sốt rét hiện nay, đồng thời chứng minh thành quả của nỗ lực hợp tác quốc tế được tiến hành từ cuối thập niên 90 thế kỷ 20 giữa các nhà khoa học thuộc các Viện Đại học Monash (Úc), Trung tâm Y khoa Nebraska (Mỹ), Viện Nhiệt đới (Thụy Sĩ) và Viện Dược phẩm Hoffmann-La Roche (Thụy Sĩ).
Sốt rét vẫn đang là gánh nặng bệnh tật của các quốc gia nhiệt đới và cận nhiệt đới khu vực sa mạc Sahara, châu Phi và Đông Nam Á và cũng là một trong những căn bệnh gây tử vong đáng kể. Mặc dù phần lớn các trường hợp sốt rét ác tính, tử vong và mắc bệnh đều quy kết cho loài ký sinh trùng sốt rét loại P.falciparum, song P. vivax cũng ảnh hưởng đến gần 100 triệu người mỗi năm trên toàn cầu. 10-20% số ca P. vivax trên toàn cầu là ở châu Phi, nam Sahara; tại vùng Đông và Nam Phi, P. vivax chiếm khoảng 10% và riêng tại Tây và Trung Phi, P. vivax chiếm dưới 1%. Ngoài châu Phi, P. vivax chiếm trên 50% và trong đó đó 80 - 90% số ca là nằm ở các quốc gia Trung Đông, châu Á, Tây Thái Bình Dương và 10 - 20% là nằm ở các quốc gia Trung và Nam Mỹ. Cùng với sốt rét do P. falciparum, thì P.vivax góp phần vào quá trình đói nghèo, tăng tỷ lệ bệnh trong mô hình bệnh tại các quốc gia ở trên; vả lại, dù không nhiều, song gần đây sốt rét do P.vivax có báo cáo là gây nên các bệnh cảnh sốt rét ác tính và tử vong, đặc biệt tại Ấn Độ, một phần không thể không nghĩ đến sự giảm đáp ứng của P. vivax với thuốc.
Tình trạng ký sinh trùng sốt rét P.falciparum kháng thuốc lan tràn nghiêm trọng trên thế giới là một khó khăn lớn cho việc lựa chọn các thuốc điều trị sốt rét. Ở Việt Nam P.falciparum kháng cao với chloroquine, Fansidar, mefloquine và giảm đáp ứng với nhiều loại thuốc chống sốt rét hiện dùng; ngay cả thuốc Artemisinine và dẫn chất Artesunate được tiến hành thử nghiệm lâm sàng và chính thức đưa vào sử dụng trong CTQGPCSR ở Việt Nam từ những năm 1990 có vai trò quan trọng trong trong việc hạ thấp tỷ lệ mắc bệnh và tử vong do sốt rét. Song, thông báo mới nhất cho biết thuốc Artemisinine đã bị kháng tại khu vực biên giới Thái Lan-Cambodia có thể làm thất bại các thành quả của chương trình phòng chống sốt rét toàn cầu và đe dọa nếu nó lan sang các quốc gia láng giềng và phạm vi rộng hơn - toàn cầu. Chloroquine là một thuốc diệt thể phân liệt mô có hiệu quả hơn 50 năm qua trong việc phòng bệnh và điều trị sốt rét do P.vivax. Mãi cho đến thập kỷ trước thuốc chloroquine vẫn còn nhạy với loài ký sinh trùng này. Song, tỷ lệ kháng cao với chloroquine đã được báo cáo lần đầu tiên tại Papua New Guinea (Rieckmann và cs., 1989), tiếp đó tại Indonesia (Baird và cs., 1991) dao động quanh 10% và nay nhiều báo cáo cho biết thực trạng kháng lan rộng khắp các vùng trên thế giới (Myat Phone Kyaw và cs., 1993; Than và cs., 1995; Garg và cs., P.T.Giáo và cs., 2002; Vinetz và cs., 2006; Teka H và cs., 2008; Tjitra E và cs., 2008; Ketama T và cs., 2009; Lee KS và cs., 2009).
Giới thiệu về đột phá phát triển thuốc điều trị sốt rét mới
Hiện nay, sốt rét vẫn là một căn bệnh khó tiêu diệt. Đặc biệt, hai loại muỗi Anopheles Gambiae và Anopheles Funesus được xem là “vô địch” trong lĩnh vực truyền bệnh sốt rét cho người ở châu Phi, làm tiêu tốn hàng năm khoảng 12 tỷ USD trong việc phòng và trị bệnh. Tại Việt Nam, mỗi năm có khoảng 1 triệu ca sốt rét, trong đó có 85% là do P. falciparum đã đề kháng với CQ và Fansidar. Vì thế, các nhà khoa học vẫn không ngừng nghiên cứu nhằm tìm ra một loại thuốc mới điều trị sốt rét hiệu quả hơn.
Bệnh sốt rét quay trở lại từ đầu thập niên 70 với các ký sinh trùng đã đề kháng nhiều loại thuốc cổ điển giá rẻ như CQ. Bệnh đã gây thiệt hại khoảng 12 tỷ USD hàng năm cho các nước châu Phi, chiếm đến 40% ngân sách phục vụ sức khỏe cộng đồng. Theo báo cáo gần đây của Viện Y học IOM thì bệnh sốt rét đang tái xuất hiện ở mức độ cao, từ đó nhấn mạnh đến việc cần thiết phải bổ sung nguồn thuốc cấp bách có thể thay thế các thuốc trị sốt rét cũ đã bị kháng với giá thành rẻ hơn. Hiện nay, liệu pháp thuốc kết hợp ACTs (Artemisinine based Combination Therapies) là phương pháp điều trị sốt rét hiệu quả nhất, nhưng do chi phí cao nên việc cung cấp cho bệnh nhân nghèo tại các địa phương có dịch sốt rét còn gặp khó khăn (mỗi năm cần tới khoảng 300-500 triệu phương thuốc điều trị).
Cây thanh hao hoa vàng đã được y học Đông phương biết đến từ lâu trong điều trị bệnh sốt rét. Tên khoa học của cây là Artemisia annua. Tại Việt Nam, hai danh y Tuệ Tĩnh và Hải Thượng Lãn Ông cũng xác nhận thanh hao hoa vàng có khả năng trị được bệnh sốt rét, chứng đổ mồ hôi trộm. Hoạt chất chính của cây thanh hao hoa vàng là Artemisinine (tiếng Trung Quốc gọi là qinghaosu) được phân lập và có cấu trúc xác định vào năm 1972 - là một chất sesquiterpene lactone với một cầu nối peroxide bên trong. Lá thanh hao được tán nhuyễn, xay thành bột để chiết xuất hoạt chất artemisinine. Năm 1993, Vonwiller và cộng sự đã báo cáo một phương pháp mới ly trích các hợp chất của cây thanh hao hoa vàng giúp gia tăng hàm lượng Artemisinine.
Việc kết hợp các dẫn xuất của artemisinin như Artesunate, Artemether tỏ ra có hiệu quả trong việc chống lại ký sinh trùng sốt rét đã đề kháng với các thuốc sốt rét cổ điển. Artemether đã được phép đăng ký sử dụng tại châu Phi với tên là Paluther. Tuy nhiên, do chi phí sản xuất thuốc còn quá cao, thời gian bán hủy ngắn nên gây nhiều khó khăn cho việc điều trị vì bệnh nhân phải dùng thuốc liên tục sau mỗi 4 giờ. Thời gian điều trị theo phác đồ kéo dài thường dễ thất bại nếu bệnh nhân không thường xuyên dùng thuốc. Mặc dù Artemisinin được xem là chất cơ bản trong liệu pháp kết hợp ACTs, nhưng “khả thi” điều trị còn giới hạn do giá thành cao cũng như phương pháp ly trích tốn nhiều thời gian. Vì thế, việc nghiên cứu sản xuất một loại thuốc hữu hiệu chống sốt rét với giá thành hạ tỏ ra cần thiết hơn bao giờ hết.
Tiến trình phát minh và cho ra đời thuốc sốt rét mới trên thế giới
Việc phát minh thuốc mới chống sốt rét là một nhu cầu thiết yếu và là nhân tố góp phần rất có ý nghĩa trong việc cứu sống hàng bao sinh mạng tại các quóc gia đang có sốt rét lưu hành, nhất là vùng sốt rét có KSTSR giảm nhạy hoặc kháng với nhiều loại thuốc sốt rét khác nhau, từ cổ điển đến những thuốc còn hiệu lực trong thời gian gần đây. Mặt khác, thuốc/ hợp chất mới đã giúp chống kháng, làm giảm tỷ lệ mắc bệnh và tỷ lệ tử vong do sốt rét rất nhiều. Lẽ đương nhiên, thuốc sốt rét mới này phải đạt được các tiêu chí sau:
rHiệu lực chống kháng và hiệu quả điều trị ưu thế hơn liệu pháp các thuốc phối hợp ACTs trước đó;
rThuốc có liệu trình ngắn, tác dụng phụ không đáng kể, khả thi áp dụng cho cộng đồng cao;
rThuốc được tổng hợp không nhất thiết phụ thuộc vào sản lượng cây thanh hao hoa vàng (lý tưởng nhất, và điều này hiện nay tại một số quốc gia và các tập đoán nghiên cứu đã cho ra sản phẩm artemisinine mà bằng các kỹ thuật hiện đại,…không nhất thiết thông qua quy trình nuôi trồng và thu hái loại cây thanh hao hoa vàng);
rGiá thành thấp cũng là một tiêu chí quan trọng.
Một số nét sơ lược về thuốc sốt rét OZ 277/Rbx 11160
Một sản phẩm mới ra đời với mã số OZ 277/Rbx 11160 đã được xem là bước đột phá lớn nhất trong điều trị sốt rét hiện nay. Đây là thành quả của một nỗ lực hợp tác quốc tế được tiến hành từ cuối thập niên 90 thế kỷ 20 giữa các nhà khoa học thuộc các Viện Đại học Monash (Úc), Trung tâm Y khoa Nebraska (Mỹ), Viện Nhiệt đới (Thụy Sĩ) và Viện Dược phẩm Hoffmann-La Roche (Thụy Sĩ). Kết quả của các công trình nghiên cứu đã được ấn bản trên tạp chí khoa học The Nature.
OZ 277/Rbx 11160 là một chất tổng hợp có cấu trúc tương tự Artemisinin, sẽ là vũ khí chính trong cuộc chiến chống lại bệnh sốt rét đa kháng thuốc và có thể đáp ứng được nhu cầu điều trị trong vòng 3 năm tới. Thuốc tác động bằng cách dùng các gốc tự do tấn công vào protein và enzyme của ký sinh trùng OZ 277/Rbx 11160 hiện đang được thử nghiệm về tính an toàn trên người với kết quả rất hứa hẹn. Giáo sư Bill Charman thuộc trường Đại học Dược Victoria cho biết OZ 277/Rbx 11160 vừa rẻ vừa dễ sản xuất, mở ra tiềm năng có thể cứu sống hàng triệu bệnh nhân sốt rét trên khắp thế giới. Theo thống kê năm 2003, mỗi ngày tại châu Phi có đến 3.000 trẻ em tử vong vì sốt rét, nghĩa là cứ mỗi 30 giây lại có một trẻ em châu Phi tử vong vì căn bệnh này. Sốt rét cũng là mối đe dọa lớn nhất đối với sức khỏe của phụ nữ có thai và trẻ sơ sinh ở châu Phi. Hiện hàng năm có khoảng 20% dân số thế giới sống ở những nước nghèo nhất phải đối diện với nguy cơ nhiễm sốt rét.
Cũng theo GS. Charman: “Chúng tôi đã thật sự xúc động về sự tiến bộ và tốc độ phát triển của thuốc. Hiện thuốc đang được thử nghiệm tại châu Âu, nếu tiến độ diễn ra tốt đẹp thì chỉ trong vòng 3 năm tới, đây sẽ là vũ khí mới giúp con người chống lại bệnh sốt rét một cách hiệu quả”. Mục đích chính của công trình nghiên cứu là cho ra đời được một loại thuốc hữu hiệu với giá thành thấp nhằm có thể cung cấp cho các quốc gia nghèo. Khả năng của OZ 277/Rbx 11160 là dùng điều trị các ký sinh trùng sốt rét đã đề kháng nhiều loại thuốc. Thử nghiệm trên chuột cho thấy hiệu lực 95-100% sạch ký sinh trùng trong vòng 3 ngày. Như thế chỉ với một đợt điều trị 3 - 4 ngày đã có thể chữa khỏi bệnh. Với giá thành điều trị 1 USD/ngày thì chương trình điều trị 3 ngày có thể dễ dàng được thực hiện. Loại thuốc mới này hứa hẹn sẽ giữ vai trò then chốt trong việc điều trị bệnh sốt rét, thay thế các thuốc cũ đã giảm hiệu quả hay đã bị kháng.
Từ tháng 5.2003, công ty dược phẩm hàng đầu của Ấn Độ Ranbaxy đã ký một thỏa ước với tổ chức MMV (Medicines for Malaria Venture) tại Geneve - Thụy Sĩ) để cùng phát triển sản phẩm peroxyde trong cuộc chiến toàn cầu chống lại bệnh sốt rét. MMV (Medicines for Malaria Venture) là tổ chức phi lợi nhuận chuyên khám phá, phát triển và phân phối các phương tiện chống sốt rét. Ngày 19/8/2004, Ranbaxy và MMV đã thông báo việc đưa thuốc vào thử nghiệm lâm sàng trên người. Cả hai đơn vị này đã được cơ quan MHPRA (Medicines and Healthcare Products Regulatory Agency) cho phép tiếp tục công việc thử nghiệm lâm sàng trên người tại Anh. Đây là bước thử nghiệm thuốc mới đầu tiên sau khi đã đạt được độ an toàn và hiệu quả trên các bước thử nghiệm tiền lâm sàng giai đoạn trước đó. OZ277/Rbx 11160 đã được lượng giá trong pha I nghiên cứu về độ an toàn, sự dung nạp cũng như hiệu lực dược lý trên người tại Anh.
Hiệu quả của thuốc OZ277 / Rbx 11160 qua một số nghiên cứu trên thế giới
1. Hoạt tính chống sốt rétcủa chất Endoperoxide tổng hợp (RBx-11160/OZ277) chống lại các phân lập Plasmodium falciparum tại Gabon
Nghiên cứu trên do nhóm tác giả Andrea Kreidenweiss, Benjamin Mordmüller, Sanjeev Krishna, Peter G. Kremsner đang làm việc tại La bô nghiên cứu y học, bệnh viện Albert Schweitzer, Lambaréné, Gabon, khoa ký sinh tùng, đại học Tübingen, Đức, Đơn vị nghiên cứu y học mức độ phân tử và tế bào, Trung tâm bệnh nhiễm trùng, St. George's, đại học London, Cranmer Terrace, London, Anh tiến hành và công bố năm 2006.
Kết quả nghiên cứu chỉ ra OZ277 là một chất mới, đây là một endoperoxide chống sốt rét hoàn toàn do tổng hợp được thử nghiệm chống lại các phân lập ký sinh trùng thu thập tại thực địa của quốc gia Gabon. Một thử nghiệm so sánh hoạt tính của OZ277 với artesunate, mefloquine và chloroquine chỉ ra OZ277 có hoạt tính chống lại tất cả phân lập ký sinh trùng rất. Artesunate và Mefloquine cũng coh thấy hoạt tính chống ký sinh tùng tiềm năng, nhưng tất cả phân lập đều kháng với chloroquine.
Một trong những trở ngại quan trọng nhất để làm giảm tỷ lệ tử vong do sốt rét là thiết lập nên các chủng kháng thuốc/ đa thuốc trong một số vùng lưu hành. Artemisinin và các dẫn suất là một phần quan trọng của các phác đồ khuyến cáo nhiều nhất vì chúng tác động chống lại các ký sinh trùng kháng. Các dấu hiệu gần đây trên in vitro kháng với một số thuốc Artemisinin và dẫn suấtlàm cho sự phát triển một thuốc mới là ưu tiên hàng đầu. Do đó, cũng không cung cấp thuốc đủ theo nhu cầu về Artemisinin vì chúng được tổng hợp từ thảo dược, nên đòi hỏi có thời gian để nuôi trồng. Vennerstrom và cộng sự đã tổng hợp một vài dẫn suất trioxolane kết hợp chặt chẽ với cầu nối endoperoxide pharmacophore của Artemisinin. Họ đã thu nhận các peroxide dạng tổng hợp với các tương tự hoặc tăng đặc tính chống sốt rét và cải thiện về đặc tính dược động học so với các dẫn suất bán tổng hợp khác.
Một hợp chất có tên OZ277 (hay gọi là trioxolane 7 và RBx-11160), là một chương trình phát triển lâm sàng. OZ277 có hoạt tính cao chống lại các chủng P. falciparum thuần chủng trong la bô và các ký sinh trùng trên loài gặm nhấm trong điều kiện in vivo. Tuy nhiên, các thử nghiệm liên quan đến các thuốc sốt rét mới chống lại các phân lập không phải trong môi trường nuôi cấy của loài P. falciparum (non-culture-adapted field isolates of P. falciparum) là rất cần thiết để đánh giá tính biến đổi của hoạt tính thuốc trong nhiều vùng khác nhaunơi mà ký sinh trùng kháng với các lớp thuốc sốt rét khác.
Các nhà nghiên ccuwus đã đồng thời kiểm tra hoạt tính của thuốc OZ277, Artesunate, chloroquine và Mefloquine trên các phân lập P. falciparum mà họ đã thu thập được trên các bệnh nhân bị sốt rét tại Lambaréné, Gabon. Hầu hết các ký sinh tùng sốt rét trong vùng này đã có mức độ kháng cao với CQ, ngược lại với mefloquine và artesunate vẫn còn hiệu quả. Các vấn đề cam kết và đánh giá hài lòng đều luôn luôn trình bày hợp pháp và có sự tham gia đánh giá của trẻ em. Sự nghiên cứu này đều có sự chấp thuận của hội đồng y đức của Tổ chức quốc tế của bệnh viện Albert Schweitzer (International Foundation of the Albert Schweitzer Hospital) ở Lambaréné. Ký sinh trùng lấy từ bệnh nhân tuổi từ 1 - 15, mắc sốt rét không biến chứng và biểu hiện nhiễm đơn thuần chỉ một loài P. falciparum (MĐKSTSR khoảng 103.1.2 x 105 KSTSR/µl) định bởi soi lam máu giem sa trên lam giọt mỏng và giọt đặc và chưa dùng thuốc sốt rét nào ít nhất một tháng. Máu tĩnh mạch được lấy 0.5ml vào trong tube chứa 16 đơn vị lithium heparin (Sarstedt) và xử lý ngay. OZ277 (trọng lượng phân tử [MW], 565) (hình ảnh trên cho thấy cấu trúc của OZ277), Artesunate (MW, 384), chloroquine diphosphate (MW, 515) và mefloquine (MW, 415) được lấy từ Medicines for Malaria Venture và hòa tan trong dimethyl sulfoxide (OZ277), 70% ethanol (artesunate), hoặc methanol (mefloquine) ở nồng độ 10 mg/ml. Chloroquine được chuẩn bị sẵn với nước cất 2 lần (5 mg/ml). Các thuốc được phân dưới dạng predose trong các plate 96 giếng vào ngày trước khi sử dụng pha loãng hàng loạt gấp 2 lần (OZ277) hoặc 3 lần cho tất cả các thuốc khác. Độ nhạy của thuốc được thử và ấn bản tài liệu trước đó, với sự cải tiến nhỏ. Mật độ KSTSR trong máu được điều chỉnh tới 0.05% với hồng cầu nhóm máu O+ từ một người cho máu khỏe mạnh, thêm vào các plate 96 giếng ở nồng độ Hct 1.5% trong môi trường nuôi cấy ký sinh trùng (RPMI 1640, 25 mM HEPES, 2 mM L-glutamine, 50 µg/ml gentamicin và 0.5% albumax), và rồi ử trong 72 giờ ở nhiệt độ 37°C trong hộp nến. Tổng số 22 mẫu đầu tiên được thử trong 3 và 1 mẫu thử trong 2 (n = 59) vì sự khác biệt giữa các giếng liên tiếp khác nhau rất thấp.
Bảng 1. Nồng độ ức chế trung bình của các thuốc nghiên cứu đối với các phân lập tại Gabon
Một lam máu giọt đặc của giếng chứng (không điều trị) được làm sau 26 giờ và đồng thời một mẫu tương tự để đông lạnh để tính sự sinh thành phần kháng nguyên HRPII (histidine-rich protein 2). Nuôi cấy ký sinh trùng được điều chỉnh thành công khi ít nhất 20% số ký sinh trùngtrưởng thành sang thể phân liệt thời điểm giờ 26. Phát triển KSTSR đươc tính từ mức độ HRPII, đo theo phương pháp thử nghiệm hiện dùng rộng rãi (MalariaAg CELISA, Cellabs, Australia). Theo quy trình đề cương của Tổ chức YTTG, chloroquine và mefloquine kháng được tính từ thể tích máu lý thuyết mà đã được chủng vào (lần lượt 1 và 5 µmol/l) vì thuốc tích tụ trong hồng cầu. Các nồng độ ức chế riêng lẻ được xác định theo phân tihcs hồi quy không tuyến tính (nonlinear regression analysis) của các đường cong đáp ứng liều thông qua bảng Curve 2D phiên bản 4 (SPSS, Inc.). Tính tương quan theo cặp đôi của các thuốc nghiên cứu được đánh giá theo hệ số Pearson của logarith giá trị nồng độ ức chế 50% đã chuyển (IC50) (JMP version 5.0.1.2; SAS Institute).
81 phân lập P. falciparum thu thập được với 50 (62%) đủ tiêu chuẩn nuôi cấy thành công. Cuối cùng, độ nhạy cảm của 38 chủng đối với thuốc OZ277, 43 chủng với Artesunate hoặc chloroquine, 44 chủng với mefloquine được thử ở đây. Các giá trị lỗi do thiếu một mẫu chứa trong quá trình vận chuyển từ Lambaréné tới Tübingen. Các sự khác biệt hay thay đổi trong thực nghiệm tối thiểu và kiểm tra chất lượng nghiêm ngặt là chủ yếu cho kiểm tra thuốc sốt rét, đặc biệt đối với các thuốc được phân chia trong các khoang của ký sinh trùng, như CQ chẳng hạn và cả OZ277. Sự bỏ sót huyết thanh người từ nuôi cấy, tương tự như bắt đầu với KSTSR trong máu và các đĩa plate rửa sạch, duy trì nồng độ hằng định trong suốt quá trình nghiên cứu (tương quan của ngày nhâp viện và hoạt độ của thuốc, r2 = 0.003; p = 0.42) theo bảng 2 dưới đây. Hệ số trung bình của việc xác định đường cong thích hợp là 0.99 (khoảng vùng phân tán giá trị là 0.98 - 1.0).
Bảng 2. Tương quan theo cặp của giá trị IC50 từ các thuốc nghiên cứu tại Gabon
Tất cả phân lập là kháng với CQ (bảng1). OZ277 chỉ ra hoạt độ thẩm thấu cao nhất, với khoảng hoạt động theo từng mẫu riêng lẻ là rất hẹp có ý nghĩa (tỷ số cao nhất đến thấp nhất của giá trị IC50, 17.2 đối với OZ277, 28.0 đối với Artesunate, 26.8 đối với CQ và 88.3 đối với Mefloquine). Điều này rất quan trọng bởi vì ngay cả một số giá trị IC50 rất cao có thể chỉ ra một nguy cơ kháng tiềm tàng. Nhạy chéo (Cross-sensitivity) được đo bằng cặp (pairwise) tương quan của giá trị IC50 log-transformed (bảng 2) giữa hoạt độ OZ277 và các thuốc khác. Điều này cao nhất với thuốc artesunate, đối so sánh là endoperoxide. Hệ số tương quan cao nhất tìm thấy giữa Artesunate và mefloquine. Ngược với Artesunate, OZ277 không tương quan thuận với Mefloquine. Tương quan giữa artesunate và OZ277 cho thấy một cơ chế chia sẻ hoạt động và đảm bảo các nghiên cứu tiếp theo để xác định lại giả thuyết này, đặc biệt nếu quan sát trên in vitro của sự kháng với artemether trở nên quan trọng về mặt lâm sàng. Thiếu mối tương quan giữa giá trị IC50 đối với OZ277 với mefloquine cũng cho thấy có sự khác trong cách artesunate có cán với KSTSR.
Tại Đông Nam Á, gia tăng số bản sao pfmdr1 là có liên quan đến tăng trị số IC50 với cả 2 thuốc mefloquine và artesunate. Tăng số bản sao pfmdr1 chưa được điều tra trong thời gian gần đây tại Lambaréné, nhưng tính đa hình amino acid trong vùng cuối của C-terminal region của Pgh1 (sản phẩm gen của pfmdr1), điều hòa tính nhạy cho artemisinin, thường ở Lambaréné. Trong khi artesunate và Mefloquine có khả năng biens đổi để tác động như một cơ chất nhờ vào vận chuyển bởi Pgh1, điều này dường như không phải là đặc điểm của OZ277. Các kết quả nghiên cứu cho thấy OZ277 có hoạt tính tuyệt vời chống lại các phân lập P. falciparum kháng CQ thu thập tại thực địa. Nó cũng là các dữ liệu từ các phân lập trong la bô và trên cả mô hình động vật và khích lệ các hướng nghiên cứu sâu hơn về thuốc mới OZ277.
2. Phát hiện sự thật về cơ chế chống sốt rét của Artemisinin và OZ277 (Arterolane) với các Nonperoxidic Isosteres và gốc Nitroxyl
Nghiên cứu trên đã được đăng tải trên tạp chí Antimicrobial Agents and Chemotherapy, số tháng 3.2010, trang 1042-1046, Volume 54, No. 3 do nhóm tác giả Matthias A. Fügi, Sergio Wittlin, Yuxiang Dong, Jonathan L. Vennerstrom thực hiện. Việc sử dụng các thử nghiệm phối hợp với nuôi cấy tế bào Plasmodium falciparum, các nhà nghiên cứu đã điều tra các tương tác của các gốc nitroxide radical spin trap, 2,2,6,6-tetramethyl-1-piperidinyloxy (TEMPO), và 4 trong số các đồng phân của chúngvới thuốc artemisinin và thuốc ozonide, ứng cử viên OZ277.
3. Đánh giá cơ chế chống sốt rét của Artemisinin và OZ277 (Arterolane) với Nonperoxidic Isosteres và gốc Nitroxyl
Nhóm tác giả Matthias A. Fügi, Sergio Wittlin, Yuxiang Dong, Jonathan L. Vennerstrom thuộc Viện Nhiệt đới Thụy Sĩ, Socinstrasse 57, CH-4002 Basel, Switzerland, đại học dược, đại học y khoa Nebraska thực hiện và ra ấn bản vào năm 2009. Kết quả nghiên cứu cho thấy thuốc chống sốt rét lọai Peroxidic như là một thuốc artemisinin bán tổng hợp có tầm quan trọng trong điều trị các trường hợp kháng thuốc. tuy nhiên, các phương thức tác động lệ thuộc cầu nối peroxide của chúng vẫn chưa hiểu biết rõ ràng.
Phối hợp dùng các thử nghiệm nuôi cấy tế bào Plasmodium falciparum, họ đã điều tra tương tác của nitroxide radical spin trap, 2,2,6,6-tetramethyl-1-piperidinyloxy (TEMPO), 4 trong số các đồng phân với artemisinin và thuốc ozonide có ứng cử viên OZ277. Chất đối kháng được quan sát đối với phối hợp của artemisinin hoặc OZ277 với đồng phân TEMPO hỗ trợ cho giả thuyết rằng sự hình thành các gốc tích carbon là quan trọng cho hoạt tính của các peroxides.
Các đồng phân TEMPO cho thấy một xu hướng chất đối kháng đối với artemisinin hơn OZ277, một điều tra có thể được giải thích bởi xu hướng các gốc carbon nguồn gốc artemisinin để thực hiện chức năng nội tại của chúng, dẫn đến một tỷ lệ thấp các gốc có sẵn cho các phản ứng hóa học tiếp sau đó như là hiện tượng alkylation của heme và các protein của KSTSR. Các nghiên cứu tiếp sau đó, họ đã thử nghiệm cả artemisinin và OZ277 trong việc phối hợp với các đồng phân nonperoxidic của chúng. Các nghiên cứu sau không hiệu quả chống sốt rét của các chất trước đây. Dữ liều này chỉ ra đặc tính chống sốt rét của peroxide không chiết suất từ các tương tác tái hồi với đích tác động của KSTSR.
4. Đánh giá trên In vitrovề các đặc tính dược học và sự phân chia của OZ277/RBx 11160 trên nuôi cấy của Plasmodium falciparum
Các tác giả Sonja Maerki, Reto Brun, Susan A. Charman, Arnulf Dorn, Hugues Matile, và Sergio Wittlin của Viện Nhiệt đới Thụy Sĩ, Socinstrasse 57, CH-4002 Basel, Switzerland, Trung Tâm chuẩn hóa các ứng cử viên thuốc, đại học Monash, Parkville, Australia và Hãng dược F. Hoffmann-La Roche, Grenzacherstrasse 124, CH-4070 Basel, Switzerland, đăng tải trên tạp chí J Med Chem. 2010 Jan 14;53(1):481-91.
Mục tiêu của nghiên cứu này là nuôi cấy synchrony loài KSTSR Plasmodium falciparum, giai đọan nhạy cảm với KSTSR đối với thuốc OZ277 (RBx-11160), đây là một chất peroxide có tính chống sốt rét được tổng hợp đầy đủ lần đầu tiên đã thử nghiệm lâm sàng phase II, dduwwjc kiểm tra in vitro qua một khoảng nòng độ 1x - 100x IC50. Thứ hai, đưa OZ277 vào trong các hồng cầu nhiễm P. falciparum (RBCs) và hồng cầu không nhiễm theo quy trình nghiên cứu in vitro thông qua đo sự phân bố của chúng giữa hồng cầu và trong huyết tương (R/P). Phương pháp nghiên cứu là đánh giá thời điểm cho tiếp xúc in vitro (1, 6, 12 hoặc 24h) với OZ277 được giám sát nhờ phối hợp với [3H]hypoxanthine trong nucleic acid của KSTSR và nhòe vào phân tích dưới KHV thường quy về đánh giá hình thể KSTSR. Nghiên cứu phân chia từng khoang được tiến hành với chất đánh dấu phóng xạ (radiolabelled) [14C]OZ277.
Kết quả cho thấy sau 1 giờ cho phơi nhiễm với OZ277 ở nồng độ cao nhất (100 x IC50) theo sau quá trình loại bỏ hợp chất, thử nghiệm hypoxanthine chỉ ra sự phát triển giai đoạn trưởng thành của P. falciparum giảm đến < 20%. Các thể nhẫn trẻ hình như ít nhạy hơn (phát triển 43%). Hồ sơ nghiên cứu liên quan đến đặc hiệu từng giao đoạn tìm thấy đối với các thuốc sốt rét tham chiếu Artemether và Chloroquine. Ức chế mạnh ( 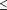 6% phát triển) của tất cả giai đoạn được quan sát khi KSTSR phơi nhiễm với mỗi trong 3 loại thuốc trong vòng 6 giờ hoặc lâu hơn. Sau khi đào thải hợp chất, KSTSR không hồi phục lại, chỉ ra sự ức chế phát triển là cơ chế gây độc tế bào (cytotoxic) hơn là kiềm hãm tế bào (cytostatic). Pyrimethamine được xác định là có hoạt tính chống lại riêng cho thể phân liệt trẻ. Phân tích hình thể qua KHV cũng cho thấy tính đặc hiệu của pyrimethamine chống lại thể phân liệt và chỉ ra OZ277, artemether và CQ làm giảm sự phát triển nhanh hơn pyrimethamine. Chỉ số R/P đối với OZ277 là 1.5 đối với các hồng cầu không nhiễm và lên đến 270 đối với các hồng cầu nhiễm.
6% phát triển) của tất cả giai đoạn được quan sát khi KSTSR phơi nhiễm với mỗi trong 3 loại thuốc trong vòng 6 giờ hoặc lâu hơn. Sau khi đào thải hợp chất, KSTSR không hồi phục lại, chỉ ra sự ức chế phát triển là cơ chế gây độc tế bào (cytotoxic) hơn là kiềm hãm tế bào (cytostatic). Pyrimethamine được xác định là có hoạt tính chống lại riêng cho thể phân liệt trẻ. Phân tích hình thể qua KHV cũng cho thấy tính đặc hiệu của pyrimethamine chống lại thể phân liệt và chỉ ra OZ277, artemether và CQ làm giảm sự phát triển nhanh hơn pyrimethamine. Chỉ số R/P đối với OZ277 là 1.5 đối với các hồng cầu không nhiễm và lên đến 270 đối với các hồng cầu nhiễm.
Nói tóm lại, nghiên cứu này cho thấy số liệu nghiên cứu đặc hiệu giai đoạn OZ277 và cho các thuốc khác như Artemether và CQ tương tự. Thứ hai, nghiên cứu mô tả một sự tích tụ có ý nghĩa của các thuốc OZ277 được đánh dầu phóng xạ trong các hồng cầu nhiễm P. falciparum.
5. Nghiên cứu sự tương quan hoạt độ - cấu trúc của thuốc Ozonide arterolane (OZ277).
Nhóm nghiên cứu gồm Dong Y, Wittlin S, Sriraghavan K, Chollet J, Charman SA, Charman WN, Scheurer C, Urwyler H, Santo Tomas J, Snyder C, Creek DJ, Morizzi J, Koltun M, Matile H, Wang X, Padmanilayam M, Tang Y, Dorn A, Brun R, Vennerstrom JL đang làm việc tại trường Đại học dược, đại học Nebraska, Omaha, Mỹ tiến hành. Kết quả cho thấy cấu trúc và cấu trúc hóa học lập thể của các thành phần cyclohexane của đồng phân của arterolane (OZ277) có hiệu quả ít chống lại P. falciparum trên in vitro. Nhóm chức năng nền yếu không đòi hỏi hiệu lực chống sốt rét phải cao, nhưng chúng cần thiết đối với hiệu lực thuốc sốt rét cao ở các con chuột nhiễm P. berghei. 5 phân tử Ozonide mới với hiệu lực chống sốt rét và hồ sơ ADME ưu thế hoặc bằng với các Arterolane đã được xác định.
6. Thuốc sốt rét chữa khỏi chỉ một liều duy nhất trên chuột
Kết quả nghiên cứu trên ấn bản vào ngày 5 tháng 4 năm 2007 cho biết các nhà hóa học Mỹ đã sử dụng y học thảo dược của Trung Quốc để tạo ra một thế hệ mới thuốc chống sốt rét có thể giải quyết một số nhược điểm đang có của các thuốc đang dùng. Gary Posner và cộng sự từ đại học Johns Hopkins, Maryland, Mỹ đã thông báo kết quả thử nghiệm lâm sàng cho thấy các hợp chất của chúng, TRIOXANES, là ứng cử viên tiềm năng đủ hiệu lực chữa khỏi các con chuột nhiễm sốt rét với liều thấp.
Những thuốc mới đều được chế tạo ra bằng cách ghép cặp với phân tử artemisinin - một sản phẩm thiên nhiên đã được sử dụng bao thế kỷ nay ở Trung Quốc để điều trị sốt rét. Liệu pháp ACTs hiện đang là hướng điều trị tốt nhất để chống lại trở ngại các chủng KSTSR kháng thuốc, thông qua điều trị phối hợp thuốc. Nhưng không phải các thuốc có góc Artemisinin hoặc chất tổng hợp trioxanes đã được báo cáo với tiềm lực có liên quan chặt chẽ với hợ chất dimer của nghiên cứu này- đó là dẫn giải của tác giả Posner. Các dimer dường như là cầu nối (bypass) diễn giải cho sự thất bại của các thuốc điều trị phối hợp dạng monomeric ACTs đang dùng, chỉ định đa liều (và trong phối hợp với các thuốc khác) để tiêu diệt KSTSR vì chúng nhanh chóng giết chết KSTSR trong máu.
Các dimer mới này hoặc là quá tiềm lực đến nỗi chúng làm sạch tất cả KSTSR trước khi chúng chuyển hóa, hoặc chúng tồn tại kéo dài trong máu. Đó là những gì các nhà nghiên cứu đang nhắm đến: chúng làm theo cấu trúc dimer để kháng hơn với sự thủy phân nhòe vào việc thay thế một liên kết acetal với cầu nối carbon-carbon mạnh hơn. Mặc dù tính an toàn của các dimer chưa được kiểm tra, song điều đó đầy hứa hẹn trong việc chữa trị các bệnh lý ung thư. Hợp chất mới này có nhiều cạnh tranh, không chỉ là toàn bộ các thuốc tổng hợp na ná như cái lõi thuốc artemisinin peroxide. Nhưng một trong số đó, OZ-277 gần đây có thành nhiều loại của khía cạnh sinh khả dụng mà hy vọng của tác giả Posner tránh được. Tổ chức Medicines for Malaria Venture (MMV), đồng tài trợ cho phát triển thuốc OZ-277 phát triển vào phase II với công ty dược Ranbaxy của Ấn Độ, Joerg Moehrle, giám đốc chương trình phát triển lâm sàng của MMV, cho biết các dữ liệu thuốc rất không ổn định trong hồng cầu của bệnh nhân nhiễm sốt rét. Jonathan Vennerstrom, đại học Trung tâm y khoa Nebraska, Omaha, Mỹ lần đầu tiên phát triển OZ-277 cho biết giờ đây ông ta đang xem xét các thuốc thế hệ thứ 2 có kéo dài trên các bệnh nhân sốt rét.
7. Tính nhạy trên in vitro của quần thể Plasmodium falciparum từ Colombia và Tanzania với một chất peroxide tổng hợp mới (OZ277)
Các tác giả Lyda Osorio, Claribel Murillo, Samanda Aponte, Valeriana Mayagaya, Christian Scheurer, Reto Brun, Hugues Matile, Sergio Wittlin đang công tác tại Trung tâm quốc tế về nghiên cứu y học và đào tạo Cali, Colombia; Trung tâm phát triển và nghiên cứu y tế Ifakara, Tanzania; Viện nhiệt đới thụy Sĩ, hãng dược phẩm hàng đầu F. Hoffmann-La Roche, Basel, Thụy Sĩ.
Kết quả nghiên cứu cho thấy tính nhạy của quần thể Plasmodium falciparum từ Colombia (n = 38) và Tanzania (n = 45) để phát triển thuốc mới, các peroxide OZ277 được tổng hợp hoàn toàn là được kiểm tra bằng cách sử dụng một bộ microtest isotopic chuẩn. OZ277 cho thấy hoạt tính chống lại các phân lập kháng CQ rất tuyệt vời ở Colombia với giá trị trung bình IC50 [khoảng] là 2.5 ng/mL [0.34–8] (4.4 nM [0.6–14]) và tại Tanzania với 1.5 ng/mL [0.22–10] (2.65 nM [0.4–17.7]). Hiệu lực của OZ277 tương tự như Artesunate, cho thấy giá trị trung bình IC50 là 1.5 ng/mL [0.42–8.6] (3.8 nM [1.1–22.3]) và 1.8 ng/mL [0.2–10] (4.7 nM [0.5–26.04]) lần lượt ở Colombia và Tanzania. Các kết quả này hỗ trợ cho sự phát triển tiếp tục của thuốc này.
Kháng với các thuốc sốt rét do Plasmodium falciparum làm cho lựa chọn hóa trị liệu ngày càng trở nên khó khăn hơn. Các thuốc phối hợp với dẫn suất artemisinin đang trở nên phát triển hơn tại các quốc gia trong và ngoài châu Phi vì các hợp chất này sinh ra một quá trình đáp ứng thuốc rất nhanh (giảm sinh khối ký sinh trùng và giải quyết nhanh các triệu chứng_reduction of the parasite biomass and resolution of symptoms), chống lại các chủng P. falciparum đa kháng thuốc, dung nạp tốt trên các bệnh nhân và giảm lượng giao bào; do vậy, chúng có tiềm năng giảm lan truyền bệnh sốt rét. Tuy nhiên, thật khó để hài hòa cùng với thế giới một cách nhanh chóng về nhu cầu artemisinin vì các hợp chất chính chiết suất từ thực vật (Artemisia annua), điều này đòi hỏi có thời gian cấy trồng. Một cách khắc phục vấn đề này là cần sinh ra thuốc chống sốt rét peroxide dạng tổng hợp đối với OZ277 là ứng cử viên dẫn đầu. OZ277 cho thấy hoạt tính trên in vitro chống lại các phân lập của P. falciparum đáp ứng trong la bô [giá trị IC50 đối với chủng nhạy CQ NF54: 0.91 ± 0.12 ng/mL đối với OZ277, so với 1.6 ± 0.1 ng/mL đối với artesunate (AS), 5.1 ± 0.8 ng/mL đối với CQ, và 5.8 ± 0.2 ng/mL đối với mefloquine (MQ)] và các loài KSTSR trên loài gặm nhấm ở môi trường in vivo. Để đánh giá sự phân bố của nồng độ ức chế trong các thể khác nhau, quần thể KSTSR tự nhiên, các nhà nghiên cứu so sánh hoạt tính trong in vitro của OZ277 với CQ, mefloquine, artesunate và methylene blue (một thuốc chống sốt rét tiềm năng được biết) trong các phân lập P. falciparum tươi lấy từ Colombia và Tanzania.
Các phân lập trên lâm sàng của P. falciparum được thu nhận với mật độ 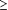 5.000/µL (~120 thể vô tính / 200 bạch cầu) từ các bệnh nhân nằm viện ở Buenaventura (B), Cali (C), Tumaco (TC), và Quibdo (QU) tại Colombia và
5.000/µL (~120 thể vô tính / 200 bạch cầu) từ các bệnh nhân nằm viện ở Buenaventura (B), Cali (C), Tumaco (TC), và Quibdo (QU) tại Colombia và 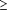 2.000/µL (50 ký sinh trùng / 200 bạch cầu) ở Ifakara tại Tanzania. Các bệnh nhân lớn hơn 7 tuổi (ở Colombia) hoặc 0.5 - 5 tuổi (ở Tanzania) có kết quả xét nghiệm nước tiểu âm tính với phản ứng Dill-Glazco test (tại Colombia) và từ chối dùng bất kỳ thuốc sốt rét nào như trong nghiên cứu. Các bệnh nhân hoặc người giám hộ phải ký vào đơn tình nguyện và bản cam kết. Nghiên cứu trên được chấp nhận bởi hội đồng Institutional Review Board của CIDEIM và hội đồng y đức (Ethics Committee of the Ifakara Health Research & Development Center). Các mẫu máu từ Tanzania và Colombia. Các lam máu nhuộm Giemsa được xét nghiệm để xác định mật độ KSTSR để xác định rằng chỉ nhiễm đơn loài P. falciparum.
2.000/µL (50 ký sinh trùng / 200 bạch cầu) ở Ifakara tại Tanzania. Các bệnh nhân lớn hơn 7 tuổi (ở Colombia) hoặc 0.5 - 5 tuổi (ở Tanzania) có kết quả xét nghiệm nước tiểu âm tính với phản ứng Dill-Glazco test (tại Colombia) và từ chối dùng bất kỳ thuốc sốt rét nào như trong nghiên cứu. Các bệnh nhân hoặc người giám hộ phải ký vào đơn tình nguyện và bản cam kết. Nghiên cứu trên được chấp nhận bởi hội đồng Institutional Review Board của CIDEIM và hội đồng y đức (Ethics Committee of the Ifakara Health Research & Development Center). Các mẫu máu từ Tanzania và Colombia. Các lam máu nhuộm Giemsa được xét nghiệm để xác định mật độ KSTSR để xác định rằng chỉ nhiễm đơn loài P. falciparum.
Máu tĩnh mạch lấy khoảng (5 mL) cho vào tube có chứa EDTA (Becton Dickinson, Cockeysville) trước khi bệnh nhân điều trị và tiến hành quy trình hoặc trong vòng 24 giờ sau khi lấy tại CIDEIM hoặc làm ngay tại Trung tâm Ifakara Health Research & Development. Tính nhạy trên in vitro với OZ277 tosylate (MW: 565), AS (MW: 384), MQ hydrochloride (MW: 415), CQ diphosphate (MW: 515) và methylene blue (MB) (MW: 374) là đo bằng thử nghiệm kết hợp cổ điển 48-giờ [3H]hypoxanthine. Tất cả hợp chất được cung cấp bởi Viện nghiên cứu nhiệt đới Swiss, ngoại trừ MB, cung cấp bởi J. Vennerstrom, Đại học Nebraska), hòa tan bởi sonication trong MSO (10 mg/mL), và giữ điều kiện 4°C cho đến khi sử dụng. Nồng độ thuốc cuối cùng cao nhất trong plate là 10 ng/mL đối với OZ277, AS, MQ, và MB và 100 ng/mL đối với CQ. Vì một số mẫu có tính nhạy thấp, nồng độ thuốc tăng nên trong suốt quá trình nghiên cứu OZ277 đến 20 ng/mL (Tanzania), MQ đến 100 ng/mL (cả 2 vùng), và CQ đến 200 ng/mL (cả 2 vùng). Các hợp chấttrước pha loãng trong môi trường sàng lọc (RPMI 1640 bổ sung với 0.5% ALBUMAX I tại Colombia và ALBUMAX II tại Tanzania, 25 mM HEPES, 25 mM NaHCO3, pH 7.3) và 100 µg/mL gentamicin ở Colombia hoặc neomycin ở Tanzania. Các hồng cầu nhiễm (100 µL/đĩa 96-well) trong Hct 2.5% vaf KSTSR trong khoảng 0.07% - 1.1% (Colombia) và từ 0.04% - 3.3% (Tanzania) được bổ sung để nhân đôi với mỗi dung dịch thuốc (100 µL, titrated hơn 64 lần). Sau 24 giờ ủ ở nhiệt độ 37°C điều kiện áp suất 5% CO2, 0.5 µCi [3H]hypoxanthine trong 50 µL của môi trường sàng lọc; các đĩa được đem đi ủ thêm 24 giờ. Các KSTSR được thu hoạch lên trên các kính lọc sợi thủy tinh (glass-fiber filters) và hoạt độ phóng xạ được tính bằng máy đếm Micro-Betaplate liquid scintillation counter (từ Wallac, Zurich, Thụy Sĩ tại Tanzania; từ Beckman, CA, ở Colombia). Các kết quả được ghi nhận đếm/ phút/ mỗi giếng tại mỗi nồng độ thuốc và trình bày như theo tỷ lệ của giếng chứng không điều trị. IC50 được ước tính bằng đường tuyến tính. Để đảm bảo chất lượng số liệu, giá trị IC50 và hệ số biến đổi > 20% và so sánh với giếng chứng duwong (KST không thuốc) là < 4x so với chuẩn (hồng cầu không nhiễm) không kết luạn trong phân tích này.
Trị số IC50 trung bình và tương ứng với khoảng được tính cho mỗi thuốc riêng biệt đối với mẫu người Colombia và Tanzania được chia thành 2 nhóm theo MĐKSTSR ban đầu (< 0.5% và 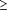 0.5%). Không IC50 có thể xác định trên một số mẫu (1/38 đối với OZ277 tại Colombia; 1/38 với AS tại Colombia, 4/38 và 11/44 đối với MQ tại cả 2 nơi; và 18/36 và 6/37 đối với CQ tại 2 nơi) khi nồng độ hợp chất bắt đầu quá thấp. Các mẫu máu không thể tương ứng như họ thử. Tương quan của các giá trị IC50 giữa OZ277 và các thuốc khác tính toán theo hệ số tương quan Spearman, giá trị p < 5% là có ý nghĩa thống kê. Tổng số 97 mẫu máu thu thập (50 tại Colombia và 47 tại Tanzania), 83 trong số này đủ tiêu chuẩn để nuôi cấy thành công. Tại Colombia, 38 mẫu có phiên giải kết quả được điều trị bằng OZ277, AS, MQ; 37 bằng MB; 36 bằng CQ. Tại Tanzania, 45 mẫu gồm trong phân tích OZ277 và AS; 44 mẫu MQ; 40 mẫu bằng CQ. MĐKSTSR trung bình nhân là 0.2% so với 0.17% trong < 0.5% nhóm và 1.09% so với 0.78% trong
0.5%). Không IC50 có thể xác định trên một số mẫu (1/38 đối với OZ277 tại Colombia; 1/38 với AS tại Colombia, 4/38 và 11/44 đối với MQ tại cả 2 nơi; và 18/36 và 6/37 đối với CQ tại 2 nơi) khi nồng độ hợp chất bắt đầu quá thấp. Các mẫu máu không thể tương ứng như họ thử. Tương quan của các giá trị IC50 giữa OZ277 và các thuốc khác tính toán theo hệ số tương quan Spearman, giá trị p < 5% là có ý nghĩa thống kê. Tổng số 97 mẫu máu thu thập (50 tại Colombia và 47 tại Tanzania), 83 trong số này đủ tiêu chuẩn để nuôi cấy thành công. Tại Colombia, 38 mẫu có phiên giải kết quả được điều trị bằng OZ277, AS, MQ; 37 bằng MB; 36 bằng CQ. Tại Tanzania, 45 mẫu gồm trong phân tích OZ277 và AS; 44 mẫu MQ; 40 mẫu bằng CQ. MĐKSTSR trung bình nhân là 0.2% so với 0.17% trong < 0.5% nhóm và 1.09% so với 0.78% trong  0.5% nhóm ở làn lượt Tanzania và Colombia.
0.5% nhóm ở làn lượt Tanzania và Colombia.
OZ277 cho thấy giá trị IC50 có thể so sánh với AS. Trong dữ liệu của họ, trong khoảng < 0.5% KSTSR, giá trị IC50 quan sát của OZ277 IC50 thay đổi từ 0.22 đến 10 (45x) tại Tanzania và 0.34 - 8 (23x) tại Colombia. Sự biến đổi này rộng hơn (18x) tìm thấy ở Gabon (0.07 - 1.26 ng/mL), nơi mà sử dụng HRP2 trong thử nghiệm in vitro test và ký sinh tùng trong máu của tất cả mẫu thuốc bình thường 0.05%. Hiệu quả của mật đọ KSTSR trong máu lên tính nhạy do P. falciparum in vitro cũng có thể sinh ra với các chủng NF54 đáp ứng trong điều kiện la bô. Điều chỉnh mật độ KSTSR trong máu đến 0.1% - 0.5% cho thử nghiệm isotopic được khuyến cáo. Do đó, khi thử các thuốc này trong điều kiện in vitro, sử dụng các mật độ tương tự có thể khác biệt này trong thực nghiệm là tối thiểu, đặc biệt đối với các thuốc mà phân khoang trong các hồng cầu nhiễm giống như CQ, artemisinin, OZ277 đã có. Các mẫu trong nhóm < 0.5% với giá trị IC50 của OZ277 là 10 ng/mL tại Tanzania (n = 1) và > 10 ng/mL tại Colombia (n = 1) có mật độ lần lượt 0.48% và 0.28%. Điều này có thể chỉ ra vấn đề kháng tồn tại trước đây, mặc dù nên chú ý rằng giá trị IC5010 ng/mL AS tại Tanzania và > 10 ng/mL tại Colombia được tìm thấy trên các phân lập khác nhau, không có dữ liệu kháng lâm sàng được báo cáo với bất kỳ AS hoặc dẫn suất nào của artemisinin.
Hầu hết các mẫu tại Colombia (34/36) và Tanzania (28/40) cho thấy giá trị IC50 > 45 ng/mL với CQ và được xếp loại như kháng. AS cho thấy giá trị IC50 thấp nhất theo sau là MB và OZ277 tại Colombia; OZ277 biểu hiện giá trị IC50 thấp nhất ở Tanzania. MB gần đây được xem là thuốc tiềm năng và được khám phá như một tác nhân phối hợp với CQ và dẫn suất Artemisinin. Dữ liệu của nghiên cứu các phân lập tại Colombia chỉ ra MB có thể là một lựa chọn hứa hẹn trong điều trị sốt rét kháng thuốc.
Có mối tương quan thuận có ý nghĩa trong các giá trị IC50 của OZ277 với tất cả các thuốc khác, ngoại trừ CQ. Tương quan giữa OZ277 và AS là r = 0.78 (p < 0.001) ở Tanzania và r = 0.45 (p = 0.006) tại Colombia và giữa OZ277 và MQ là r = 0.48 (p = 0.001) tại Tanzania và r = 0.62 (p < 0.001) tại Colombia. Tương quan giữa OZ277 và AS không đáng ngạc nhiên vì cả hai phân tử đều là peroxide, do vậy chúng có thể cùng chung một cơ chế tác động.
Tương quan tương tự được thấy sớm hơn ở các phân lập thu được từ người Gabon nhiễm P. falciparum. Tuy nhiên, tương quan thuận giữa nhạy cảm trên in vitro của OZ277 và MQ, điều này thấy ở cả hai nơi, nhưng không thấy ở Gabon. Sự quan sát này nên lưu ý và có thể có liên quan do sự hiện diện của kháng MQ, đặc biệt tại khu vực Đông Nam Á. Mặt khác, ý nghĩa lâm sàng của tương quan này có thể thấp vì AS và MQ cũng cho thấy tương quan thuận chiểu trên in vitro nhưng hiệu lực điều trị cao khi dùng thuốc dạng phối hợp.
Các nhà nghiên cứu kết luận rằng các kết quả trên in vitro chỉ ra OZ277 có hoạt tính chống lại KSTSR rất tuyệt vời, các phân lập kháng CQ của P. falciparum thu nhận trên thực địa. Điều này càng thêm củng cố các dữ liệu trên in vitro lấy được từ các phân lập phòng thí nghiệm và từ mô hình động vật. cũng như cong trình trước đây thực hiện với các phân lập P. falciparum tại thực địa từ các vùng khác. Điều cần thiết là chuẩn hóa mật độ KSTSR ban đầu để so sánh hiệu lực trên in vitro của OZ277 tại các vùng khác nhau.
Như vậy, trong vòng vài năm tới, chúng ta hy vọng con người sẽ có thêm một vũ khí hữu hiệu để ngăn chặn bệnh sốt rét, đặc biệt là xử trí chống kháng tốt - bệnh sốt rét hiện vẫn là nỗi lo của những quốc gia chậm hoặc đang phát triển, đặc biệt vấn đề hiện nay chúng ta vẫn chưa có một vaccine hữu hiệu nào khác cho phòng sốt rét hiệu quả.
Tài liệu tham khảo
1.Kremsner P, Krishna S, 2004. Antimalarial combinations. Lancet 364: 285–294.
2.Woodrow CJ, Haynes RK, Krishna S, 2005. Artemisinins. Postgrad Med J 81: 71–78.
3.Vennerstrom J, Arbe-Barnes S, Brun R, Charman S, Chlu F, Chollet J, Dong Y, Dorn A, Hunziker D, Matile H, McIntosh K, Padmanilayam M, Santo-Tomas J, Scheurer C, Scorneaux B, Tang Y, Urwyler H, Wittlin S, Charman W, 2004. Identification of an antimalarial synthetic trioxolane drug development candidate. Nature 430: 900–904.
4.Churchill F, 1989. Field adapted assays for chloroquine and its metabolites in urine and blood. Parasitol Today 5: 116, 121–126.
5.Desjardins RE, Canfield CJ, Haynes JD, Chulay JD, 1979. Quantitative assessment of antimalarial activity in vitro by a semiautomated microdilution technique. Antimicrob Agents Chemother 16: 710–718.
6.Huber W, Koella J, 1993. A comparison of three methods of estimating EC50 in studies of drug resistance of malaria parasites. Acta Trop 55: 257–261.
7.Kreidenweiss A, Mordmüller B, Krishna S, Kremsner PG, 2006. Antimalarial activity of a synthetic endoperoxide (RBx-11160/ OZ277) against Plasmodium falciparum isolates from Gabon. Antimicrob Agents Chemother 50: 1535–1537.
8.Basco L, 2004. Molecular epidemiology of malaria in Cameroon. XX. Experimental studies on various factors of in vitro drug sensitivity assays using fresh isolates of Plasmodium falciparum. Am J Trop Med Hyg 70: 474–480.
9.Verdier F, Le Bras J, Clavier F, Hatin I, Blayo M-C, 1985. Chloroquine uptake by Plasmodium falciparum-infected human erythrocytes during in vitro culture and its relationship to chloroquine resistance. Antimicrob Agents Chemother 27: 561–564.
10.Vyas N, Avery B, Avery M, Wyandt C, 2002. Carrier-mediated partitioning of artemisinin into Plasmodium falciparum-infected erythrocytes. Antimicrob Agents Chemother 46: 105–109.
11.Gu H, Warhurst D, Peters W, 1984. Uptake of [3H]dihydroartemisinin by erythrocytes infected with Plasmodium falciparum in vitro. Trans R Soc Trop Med Hyg 78: 265–270.
12.Maerki S, Brun R, Charman S, Dorn A, Matile H, Wittlin S, 2006. In vitro assessment of the pharmacodynamic properties and the partitioning of OZ277/RBx-11160 in cultures of Plasmodium falciparum. J Antimicrob Chemother 58: 52–58.
13.Cerutti C Jr, Marques C, Alencar FE, Durlacher RR, Alween A, Segurado AA, Pang LW, Zalis MG, 1999. Antimalarial drug susceptibility testing of Plasmodium falciparum in Brazil using a radioisotope method. Mem Inst Oswaldo Cruz 94: 803–809.
14.Akoachere M, Buchholz K, Fischer E, Burhenne J, Haefeli W, Schirmer R, Becker K, 2005. In vitro assessment of methylene blue on chloroquine-sensitive and -resistant Plasmodium falciparum strains reveals synergistic action with artemisinins. Antimicrob Agents Chemother 49: 4592–4597.
15.Brockman A, Price R, van Vugt M, Heppner D, Walsh D, Sookto P, Wimonwattrawatee T, Looareesuwan S, White N, Nosten F, 2000. Plasmodium falciparum antimalarial drug susceptibility on the north-western border of Thailand during five years of extensive use of artesunatemefloquine. Trans R Soc Trop Med Hyg 94: 537–544.